Hvordan påvirkede Atom -forskning udført af John Dalton Sir Joseph Thomson Ernest Rutherford og Niels Bohr videnskabelig tanke gennem hele videnskabens historie?
John Dalton (1803):
* Daltons atomteori: Dalton foreslog, at elementer er sammensat af udelelige partikler kaldet atomer. Denne teori, der er baseret på eksperimentelle observationer, gav et fundament for forståelse af kemiske reaktioner og materialens egenskaber.
* påvirkning: Daltons teori etablerede begrebet atomer som den mindste stofenhedsenhed og revolutionerede forståelsen af kemisk sammensætning og banede vejen for yderligere atomforskning.
J.J. Thomson (1897):
* Opdagelse af elektronet: Thomson opdagede elektronet, en negativt ladet partikel, der var meget mindre end atomet. Denne opdagelse udfordrede Daltons idé om udelelige atomer.
* blomme budding model: Thomson foreslog modellen "blomme budding", hvilket antydede, at atomet var en sfære med positiv ladning med negativt ladede elektroner indlejret i.
* påvirkning: Thomsons opdagelse af elektronet og hans model ændrede signifikant forståelsen af atomstruktur, introducere ideen om subatomiske partikler og banede vejen for yderligere undersøgelse af atomets interne struktur.
Ernest Rutherford (1911):
* nuklear model: Rutherford opdagede gennem sit berømte guldfolieeksperiment kernen, en tæt, positivt ladet region i midten af atomet. Han foreslog den nukleare model, hvilket antydede, at elektroner kredsede omkring kernen.
* påvirkning: Rutherfords model revolutionerede forståelsen af atomstruktur og etablere kernen som den centrale og mest massive del af atomet, der var ansvarlig for dets positive ladning. Denne opdagelse lagde grundlaget for yderligere atomforskning, herunder udvikling af nuklear fysik.
Niels Bohr (1913):
* Bohr Model: Bohr foreslog en model af atomet, hvor elektroner kredser om kernen i specifikke energiniveauer eller skaller. Han forklarede linjespektre for elementer ved at antyde, at elektroner kunne hoppe mellem energiniveauet, udsende eller absorbere lys.
* påvirkning: Bohrs model gav en mere nøjagtig beskrivelse af atomstruktur end Rutherfords og forklarede elementernes spektrale egenskaber. Det lagde grunden til udvikling af kvantemekanik, et stort gennembrud i fysik, der revolutionerede vores forståelse af atomet og dets egenskaber.
samlet påvirkning:
Undersøgelsen af Dalton, Thomson, Rutherford og Bohr lagde grundlaget for vores moderne forståelse af atomet. Deres arbejde førte til udviklingen af:
* Moderne kemi: Begrebet atomer og deres egenskaber muliggjorde udvikling af moderne kemi, herunder den periodiske tabel og kemiske binding.
* nuklear fysik: Rutherfords opdagelse af kernen åbnede døren til området for nuklear fysik, hvilket førte til forståelsen af radioaktivitet, nukleare reaktioner og atomenergi.
* kvantemekanik: Bohrs arbejde banede vejen for udviklingen af kvantemekanik, der revolutionerede forståelsen af stof på atom- og subatomiske niveauer.
Disse opdagelser påvirkede dybtgående videnskabelig tanke, hvilket førte til fremskridt inden for forskellige områder og former vores forståelse af universet på det mest grundlæggende niveau.
Sidste artikelHvilket antal angiver, hvor optisk tæt stof er?
Næste artikelHvad er materialer, der tillader elektroner at flyde frit kaldet?
 Varme artikler
Varme artikler
-
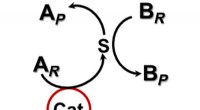 Accelererer kemiske reaktioner uden direkte kontakt med en katalysatorEt berøringsfrit katalytisk system. Kredit: Videnskabens fremskridt (2020). DOI:10.1126/sciadv.aax6637 Et forskerhold fra Northwestern University har afsløret en ny tilgang til at udføre kemiske
Accelererer kemiske reaktioner uden direkte kontakt med en katalysatorEt berøringsfrit katalytisk system. Kredit: Videnskabens fremskridt (2020). DOI:10.1126/sciadv.aax6637 Et forskerhold fra Northwestern University har afsløret en ny tilgang til at udføre kemiske -
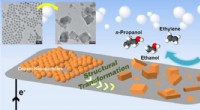 Kobberkatalysator giver højeffektiv CO2-til-brændstofkonverteringSkematisk af en ny katalysator lavet af kobbernanopartikler, der omdanner kuldioxid til multicarbonprodukter (ethylen, ethanol, og propanol). Øverst til venstre er transmissionselektronmikroskopbilled
Kobberkatalysator giver højeffektiv CO2-til-brændstofkonverteringSkematisk af en ny katalysator lavet af kobbernanopartikler, der omdanner kuldioxid til multicarbonprodukter (ethylen, ethanol, og propanol). Øverst til venstre er transmissionselektronmikroskopbilled -
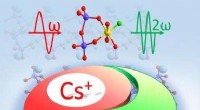 Forskning afdækker det første ikke-centrosymmetriske fluorooxosilicophosphat med Si-F-bindingerSkematisk illustration af forskningen. Kredit:Prof. LUOs gruppe Dyb-ultraviolette (UV) ikke-lineære optiske materialer spiller en afgørende rolle i en række forskellige højteknologiske videnskabel
Forskning afdækker det første ikke-centrosymmetriske fluorooxosilicophosphat med Si-F-bindingerSkematisk illustration af forskningen. Kredit:Prof. LUOs gruppe Dyb-ultraviolette (UV) ikke-lineære optiske materialer spiller en afgørende rolle i en række forskellige højteknologiske videnskabel -
 Ny teknik muliggør rumlig adskillelse af peptidstrukturerForskellige 3D-strukturer af biologiske molekyler, for eksempel et dipeptid med to forskellige konformationer vist som rødt og blåt, kan rumligt adskilles ved at skyde en kold molekylær stråle gennem
Ny teknik muliggør rumlig adskillelse af peptidstrukturerForskellige 3D-strukturer af biologiske molekyler, for eksempel et dipeptid med to forskellige konformationer vist som rødt og blåt, kan rumligt adskilles ved at skyde en kold molekylær stråle gennem
- Tilfældig registrering af en årlig massefremkomst af gådefulde mantisfluer
- Snesevis af forhistoriske, Romerske og middelalderlige steder opdaget af arkæologiske frivillige, d…
- Bjørne er ikke generet af kost med højt mættet fedt
- Hvilke kemikalier har jorden og månen til fælles?
- Hvad er produktet af denne ligning (NH4) (NO3) plus (C4H6O2)?
- Hvad er stjernen i midten af solsystemet, hvor jord og anden sag kredserer?


