Hvorfor danner atomer af ikke -metaller anioner, mens metalkationer?
1. Elektronkonfiguration:
* Metaller: Metaller har generelt et par elektroner i deres yderste skal (Valence Shell). De har en tendens til at miste disse elektroner for at opnå en stabil elektronkonfiguration, der ofte ligner den nærmeste ædle gas. At miste elektroner skaber en positiv ladning hvilket resulterer i en kation.
* ikke -metaller: Ikke -metaller har mange elektroner i deres ydre skal, ofte tæt på en fuld skal. De har en tendens til at få elektroner for at afslutte deres ydre skal og opnå en stabil elektronkonfiguration som en ædel gas. At vinde elektroner skaber en negativ ladning , hvilket resulterer i en anion.
2. Elektronegativitet:
* Metaller: Metaller har typisk lav elektronegativitet, hvilket betyder, at de har en svagere attraktion for elektroner. Dette gør dem mere tilbøjelige til at miste elektroner og blive kationer.
* ikke -metaller: Ikke -metaller har høj elektronegativitet, hvilket indikerer en stærk tiltrækning for elektroner. Dette gør dem mere tilbøjelige til at få elektroner og blive anioner.
3. Ioniseringsenergi:
* Metaller: Metaller har relativt lave ioniseringsenergier, hvilket betyder, at det kræver mindre energi at fjerne et elektron. Dette gør dem mere tilbøjelige til at miste elektroner og blive kationer.
* ikke -metaller: Ikke -metaller har høje ioniseringsenergier, hvilket kræver mere energi til at fjerne en elektron. Dette gør dem mindre tilbøjelige til at miste elektroner og mere tilbøjelige til at få elektroner og blive anioner.
Eksempel:
* natrium (NA): Natrium er et metal med en valenselektron. Det mister let denne elektron for at blive en Na+ -kation og opnå den stabile elektronkonfiguration af neon (NE).
* klor (Cl): Chlor er en ikke -metal med syv valenselektroner. Det får let en elektron for at blive en Cl-anion og opnå den stabile elektronkonfiguration af argon (AR).
Kortfattet:
Metallers tendens til at miste elektroner og ikke -metaller for at få elektroner er drevet af deres ønske om at opnå en stabil elektronkonfiguration. Denne forskel i elektronadfærd afspejles i deres elektronegativitet, ioniseringsenergi og fører i sidste ende til dannelse af kationer for metaller og anioner for ikke -metaller.
Sidste artikelHvilke materialer er lavet af gode ledere?
Næste artikelHvor dybde og densitet påvirker væske?
 Varme artikler
Varme artikler
-
 C9h -peptid er begrænset til at fremkalde kræftcelle -apoptoseKredit:Asociación RUVID Forskere ved Valencias Universitat Politècnica (UPV), Valencia-CSIC Biomedicine Institute (IBV) og Bioengineering, Biomateriale og nanomedicin CIBER (CIBER BBN) har udvikle
C9h -peptid er begrænset til at fremkalde kræftcelle -apoptoseKredit:Asociación RUVID Forskere ved Valencias Universitat Politècnica (UPV), Valencia-CSIC Biomedicine Institute (IBV) og Bioengineering, Biomateriale og nanomedicin CIBER (CIBER BBN) har udvikle -
 Forskere udvikler nye, lavprisværktøj til påvisning af bakterier i mad og vandKredit:University of Massachusetts Amherst Fødevareforsker Lili He og kolleger ved University of Massachusetts Amherst rapporterer, at de har udviklet en ny, hurtig og billig metode til påvisning
Forskere udvikler nye, lavprisværktøj til påvisning af bakterier i mad og vandKredit:University of Massachusetts Amherst Fødevareforsker Lili He og kolleger ved University of Massachusetts Amherst rapporterer, at de har udviklet en ny, hurtig og billig metode til påvisning -
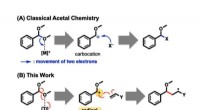 Radikal kemi muliggør ligetil syntese af ethereFigur 1. Aktiveringstilstand for acetaler. (A) Klassisk, acetal C-O-bindinger spaltes på heterolytisk vis. To elektroner, der udgør en C-O-binding, fjernes begge af en sur aktivator ([M]+) for at tilv
Radikal kemi muliggør ligetil syntese af ethereFigur 1. Aktiveringstilstand for acetaler. (A) Klassisk, acetal C-O-bindinger spaltes på heterolytisk vis. To elektroner, der udgør en C-O-binding, fjernes begge af en sur aktivator ([M]+) for at tilv -
 Ny tilgang vil hjælpe med at identificere lægemidler, der kan lime proteiner sammenKredit:Pixabay/CC0 Public Domain En ny screeningsmetode, der kan teste effektiviteten af terapeutiske molekyler designet til at lime proteiner sammen i kroppen, er udviklet af forskere ved Unive
Ny tilgang vil hjælpe med at identificere lægemidler, der kan lime proteiner sammenKredit:Pixabay/CC0 Public Domain En ny screeningsmetode, der kan teste effektiviteten af terapeutiske molekyler designet til at lime proteiner sammen i kroppen, er udviklet af forskere ved Unive
- Et samfunds fækale sag kan give tidlig advarsel om COVID-19-udbrud, undersøgelse finder
- Hvad er de to hovedtilstande med blank energi kinetisk og potentiel energi?
- Hvilket grundlæggende element blandes med glukose for at skabe energi?
- Hvad hedder et sandbjerge virkelig?
- UVeye køretøjsinspektionssystem jagter det underlige til det sørgelige
- Siden et øjeblik er krafttider afstand, det er sandt at kalde kraft?


