I den aktuelle model af atomelektroner er der placeret i?
Her er hvorfor:
* Bohr -modellen: Den gamle model af atomet, kendt som Bohr -modellen, afbildede elektroner, der kredser om kernen i faste, cirkulære stier som planeter omkring solen. Denne model betragtes ikke længere som nøjagtig.
* Den kvantemekaniske model: Den aktuelle model, kaldet den kvantemekaniske model, beskriver elektroner som eksisterende i sandsynlighedsskyer , ikke faste stier. Disse skyer repræsenterer regionerne, hvor et elektron mest sandsynligt findes. Disse regioner kaldes orbitaler .
* orbitaler: Orbitaler er ikke flade, cirkulære stier. De er komplekse, tredimensionelle former, der definerer sandsynligheden for at finde en elektron i en bestemt rumområde omkring kernen. Forskellige orbitaler har forskellige former og energiniveau.
Så selvom vi ikke kan sige nøjagtigt, hvor et elektron er på ethvert givet tidspunkt, kan vi beskrive sandsynligheden for at finde det i en bestemt region omkring kernen ved hjælp af begrebet elektronskyer eller orbitaler.
Sidste artikelHvad er forskellen mellem fysiske egenskaber og kemiske egenskaber?
Næste artikelHvad bidrog Schrodinger i atomets historie?
 Varme artikler
Varme artikler
-
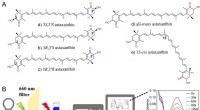 Forskelle fundet i antioxidantaktiviteter af astaxanthinisomerer mod singlet oxygen(A) Strukturer af stereoisomerer af astaxanthin. (B) Måling af singlet-iltslukningskapaciteten af antioxidanter. Kredit:Zheng Xinxin For nylig foreslog forskere ledet af prof. Huang Qing fra Inst
Forskelle fundet i antioxidantaktiviteter af astaxanthinisomerer mod singlet oxygen(A) Strukturer af stereoisomerer af astaxanthin. (B) Måling af singlet-iltslukningskapaciteten af antioxidanter. Kredit:Zheng Xinxin For nylig foreslog forskere ledet af prof. Huang Qing fra Inst -
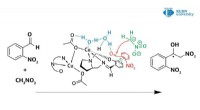 Vand spiller en afgørende rolle i mekanismen for Henry-reaktionen katalyseret af nye kobberkompleks…Kredit:RUDN Universitet En kemiker fra RUDN University reviderede mekanismen for Henry-reaktionen katalyseret af kobber(II)-komplekser. Dermed, ved hjælp af nye kobber(II)-komplekser opnået i samm
Vand spiller en afgørende rolle i mekanismen for Henry-reaktionen katalyseret af nye kobberkompleks…Kredit:RUDN Universitet En kemiker fra RUDN University reviderede mekanismen for Henry-reaktionen katalyseret af kobber(II)-komplekser. Dermed, ved hjælp af nye kobber(II)-komplekser opnået i samm -
 Gennemstrømningselektroder gør brint 50 gange hurtigereEt eksempel på de små, gennemstrømningselektrode, som Duke-forskere brugte til at producere mere brint fra elektrolyse med en krone til skala. Kredit:Wiley Lab, Duke University Elektrolyse, passer
Gennemstrømningselektroder gør brint 50 gange hurtigereEt eksempel på de små, gennemstrømningselektrode, som Duke-forskere brugte til at producere mere brint fra elektrolyse med en krone til skala. Kredit:Wiley Lab, Duke University Elektrolyse, passer -
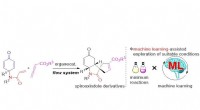 En vanskelig reaktionssekvens får et stort løft fra et flow-opsætning og statistikMaskinstøttet udforskning af organokatalyseret dominoreaktion i flowsystem. Kredit:Royal Society of Chemistry Forskere fra Osaka University optimerer en kompliceret dominoreaktion i et flowsystem
En vanskelig reaktionssekvens får et stort løft fra et flow-opsætning og statistikMaskinstøttet udforskning af organokatalyseret dominoreaktion i flowsystem. Kredit:Royal Society of Chemistry Forskere fra Osaka University optimerer en kompliceret dominoreaktion i et flowsystem
- At stille retshåndhævende myndigheder til ansvar for elektronisk overvågning
- Vil du lette stresset ved nedskæringer? Hold billeder, mindeværdige ting, siger forskning
- Australien bebrejder virksomhederne for langsom reaktion på Solomons olieudslip
- Ændrer inertien af et objekt, når hastigheden ændrer sig?
- Hvorfor bliver mit hår grønt fra swimmingpoolen?
- NASA ser Tropical Cyclone Debbie nærme sig Queensland for landgang


