Hvad er nogle metalliske bindinger?
Her er en sammenbrud:
* Hvad er metalliske bindinger? Metalliske bindinger er en type kemisk binding, der forekommer mellem atomer af metaller. De involverer deling af et "hav" af delokaliserede elektroner blandt et gitter af positivt ladede metalioner. Disse delokaliserede elektroner er ikke bundet til noget specifikt atom og kan bevæge sig frit gennem metalstrukturen.
* Hvorfor er metalliske obligationer unikke?
* stærk og ikke-retningsbestemt: Metalliske bindinger er stærke, hvilket forklarer de høje smeltepunkter og kogepunkter for metaller. De er også ikke-retningsbestemte, hvilket betyder, at elektronerne kan bevæge sig i enhver retning inden for metalstrukturen. Dette giver metaller deres formbarhed (evne til at formes) og duktilitet (evne til at blive trukket ind i ledninger).
* Hav af elektroner: De delokaliserede elektroner skaber et "hav" med negativ ladning, der omgiver de positivt ladede metalioner. Dette forklarer metallers gode elektriske og termiske ledningsevne. De frit bevægende elektroner kan let bære elektrisk strøm, og de kan også overføre varmeenergi effektivt.
* Metallisk glans: Interaktionen mellem lys og de delokaliserede elektroner giver metaller deres karakteristiske skinnende udseende.
Eksempler på metaller med metallisk binding:
* jern (Fe)
* kobber (cu)
* guld (AU)
* aluminium (AL)
* sølv (AG)
* natrium (NA)
* magnesium (mg)
Det er vigtigt at bemærke, at dette kun er et par eksempler, og mange andre metaller udviser metallisk binding.
I stedet for specifikke "metalliske bindinger", er den vigtigste takeaway at forstå konceptet med metallisk binding selv, der forklarer metallers unikke egenskaber.
Sidste artikelHvad gør nogle materialer til gode varmeafdelinger?
Næste artikelHvilken har mindre tæthed en kork eller vand?
 Varme artikler
Varme artikler
-
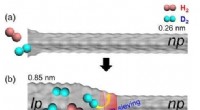 Ny strategi for isotopadskillelse med fleksibelt porøst materialevejrtrækning af MIL-53(Al), en fleksibel metal-organisk ramme (MOF). Kredit:UNIST En ny undersøgelse foretaget af et internationalt hold af forskere tilknyttet UNIST er lykkedes med at udvikle en
Ny strategi for isotopadskillelse med fleksibelt porøst materialevejrtrækning af MIL-53(Al), en fleksibel metal-organisk ramme (MOF). Kredit:UNIST En ny undersøgelse foretaget af et internationalt hold af forskere tilknyttet UNIST er lykkedes med at udvikle en -
 Forskere udvikler en katalysator til at lette selektiv omdannelse af reaktive lithiumforbindelserBochums forskningsteam har udviklet en ny katalysator, der kunne være interessant til industrielle anvendelser. Kredit:RUB, Marquard Forskere ved Ruhr-Universität Bochum har udviklet en ny katalys
Forskere udvikler en katalysator til at lette selektiv omdannelse af reaktive lithiumforbindelserBochums forskningsteam har udviklet en ny katalysator, der kunne være interessant til industrielle anvendelser. Kredit:RUB, Marquard Forskere ved Ruhr-Universität Bochum har udviklet en ny katalys -
 Lys og peptider:Ny metode diversificerer livets naturlige byggestenSollys eksperiment. Reaktionerne kan udføres ved hjælp af lyset fra solen i en enkel glaskolbe. Kredit:J. Waser/EPFL Opdagelse af nye biologiske mål er en kritisk del af vores igangværende kamp mo
Lys og peptider:Ny metode diversificerer livets naturlige byggestenSollys eksperiment. Reaktionerne kan udføres ved hjælp af lyset fra solen i en enkel glaskolbe. Kredit:J. Waser/EPFL Opdagelse af nye biologiske mål er en kritisk del af vores igangværende kamp mo -
 Oprettelse af lithium-ion-batterier med højere energitæthed til vedvarende energianvendelserI den Journal of Vacuum Science and Technology A , forskere undersøger oprindelsen af nedbrydning i LIB-katodematerialer med høj energitæthed og udvikler strategier til at afbøde disse nedbrydning
Oprettelse af lithium-ion-batterier med højere energitæthed til vedvarende energianvendelserI den Journal of Vacuum Science and Technology A , forskere undersøger oprindelsen af nedbrydning i LIB-katodematerialer med høj energitæthed og udvikler strategier til at afbøde disse nedbrydning
- Kvantefysikbegrebet kritisk masse
- Ud over likes, delinger og kommentarer:Hvordan kan brands bruge sociale medier til at stimulere båd…
- Området med to nærliggende tektoniske plader bevæger sig væk fra hinanden kaldes en hvilken græ…
- Forskere opdager en ny måde at helbrede defekter i materialer på
- Tornado advarsel? I øst bringer stormsæsonen forvirring (Opdatering)
- Hvad hedder visse fødevarer, der hjælper med at beskytte celler mod skader?


