Når salt opløses i vand, hvad dannede det sig?
* natriumioner (Na+)
* chloridioner (Cl-)
Her er en sammenbrud af, hvad der sker:
1. Polaritet: Vandmolekyler er polære, hvilket betyder, at de har en lidt positiv ende (nær brintatomerne) og en lidt negativ ende (nær iltatomet).
2. attraktion: Den positive ende af vandmolekyler tiltrækkes af de negative chloridioner (Cl-), mens den negative ende af vandmolekyler tiltrækkes af de positive natriumioner (Na+).
3. dissociation: Disse attraktioner overvinder den ioniske binding, der holder natrium- og chloridioner sammen i saltkrystallen. Ionerne adskiller sig og bliver omgivet af vandmolekyler, der danner det, der kaldes A hydreringsskal .
Så når salt opløses i vand, forsvinder det ikke; Det bryder simpelthen ned i individuelle ioner, der er omgivet af vandmolekyler. Denne proces kaldes elektrolytdissociation Fordi den resulterende løsning kan udføre elektricitet.
Sidste artikelHvilket antal carbonatomer er i acetyl CoA?
Næste artikelReaktionen katalyseret af DNA -polymerase er?
 Varme artikler
Varme artikler
-
 Hvad er det hvide på min påskechokolade, og kan jeg stadig spise det?Kredit:Shutterstock Ordene chokolade og skuffelse går ikke ofte sammen. Men du har måske oplevet en vis skuffelse, hvis du nogensinde har pakket den lyse folie af et påskeæg ud for at opdage hvid,
Hvad er det hvide på min påskechokolade, og kan jeg stadig spise det?Kredit:Shutterstock Ordene chokolade og skuffelse går ikke ofte sammen. Men du har måske oplevet en vis skuffelse, hvis du nogensinde har pakket den lyse folie af et påskeæg ud for at opdage hvid, -
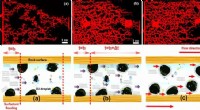 En ny klasse af forgrenede enkeltkædede overfladeaktive stoffer til forbedret olieudvinding rapport…Øverst:Forskelle i bevægelsen af olie gennem mikrokanalerne efter opløsningens oversvømmelse af (a) ren saltlage, b) rent overfladeaktivt stof og (c) overfladeaktivt middel-saltvand. Nederst:Skemati
En ny klasse af forgrenede enkeltkædede overfladeaktive stoffer til forbedret olieudvinding rapport…Øverst:Forskelle i bevægelsen af olie gennem mikrokanalerne efter opløsningens oversvømmelse af (a) ren saltlage, b) rent overfladeaktivt stof og (c) overfladeaktivt middel-saltvand. Nederst:Skemati -
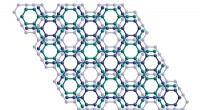 Langhypoteseret næste generations vidundermateriale skabt for første gangKrystalstrukturen af et lag af grafyn. Kredit:Yiming Hu I over et årti har forskere forsøgt at syntetisere en ny form for kulstof kaldet grafyn med begrænset succes. Den bestræbelse er dog nu ved
Langhypoteseret næste generations vidundermateriale skabt for første gangKrystalstrukturen af et lag af grafyn. Kredit:Yiming Hu I over et årti har forskere forsøgt at syntetisere en ny form for kulstof kaldet grafyn med begrænset succes. Den bestræbelse er dog nu ved -
 Video:Petrichor, lugten af regnKredit:The American Chemical Society Duften, der ledsager en forårsbyge, er så stemningsfuld, at den har sit eget ord:petrichor. Se, mens Reactions udforsker den unikke kemi bag lugten af regn:
Video:Petrichor, lugten af regnKredit:The American Chemical Society Duften, der ledsager en forårsbyge, er så stemningsfuld, at den har sit eget ord:petrichor. Se, mens Reactions udforsker den unikke kemi bag lugten af regn:
- Hvad er vigtigheden af bevaring?
- Projektbaseret læring giver bedre elevresultater
- Forskel mellem kvarts og Calcite
- Undersøgelse sætter spørgsmålstegn ved bæredygtigheden af planteingredienser som fiskemelsubs…
- Vulkanaktiviteten stopper ved Hawaii-krateret, men der forventes flere udbrud
- Hvad Mælkevejen Galaxy løber gennem midten af konstellationen?


