Hvilken binding øger en atomer stabilitet?
* octet regel: De fleste atomer stræber efter at opnå en stabil elektronkonfiguration, der ofte ligner de ædle gasser med deres fulde ydre skal af elektroner. For de fleste atomer betyder det at have otte elektroner i deres yderste skal (oktetreglen).
* Deling af elektroner: Kovalente bindinger dannes, når atomer deler elektroner for at opnå en stabil oktet. Ved at dele elektroner "udfylder begge atomer, der er involveret i bindingen, effektivt" deres ydre skaller, hvilket øger deres stabilitet.
Eksempel:
* Overvej et hydrogenatom (H) med kun en elektron. Det har brug for endnu en elektron for at have en stabil konfiguration. Når to hydrogenatomer binder sig kovalent, deler de deres elektroner og danner et brintmolekyle (H2). Hvert hydrogenatom har nu effektivt to elektroner i sin ydre skal og opnå en stabil konfiguration.
Andre typer obligationer:
* ioniske bindinger: Disse bindinger involverer overførsel af elektroner, hvor et atom mister en elektron og en anden får en. Mens ioniske bindinger kan føre til stabilitet, er de ikke så stærke som kovalente bindinger generelt.
* Metalliske obligationer: Disse bindinger forekommer i metaller, hvor elektroner delokaliseres på tværs af et gitter af atomer. Mens de bidrager til de unikke egenskaber ved metaller, involverer de ikke nødvendigvis den samme form for elektrondeling, der fører til oktetreglen.
 Varme artikler
Varme artikler
-
 At lave rent brint er svært, men forskere har lige løst en stor forhindringHoldets eksperimentelle vandopdelingsapparat. Kredit:Cockrell School of Engineering, University of Texas i Austin I årtier, forskere rundt om i verden har søgt efter måder at bruge solenergi til a
At lave rent brint er svært, men forskere har lige løst en stor forhindringHoldets eksperimentelle vandopdelingsapparat. Kredit:Cockrell School of Engineering, University of Texas i Austin I årtier, forskere rundt om i verden har søgt efter måder at bruge solenergi til a -
 Fluorescerende molekyler afsløret af kvantekemi og maskinlæringOtte forbindelser blev forudsagt at fluorescere ved en ny metode til design af molekyler. Af de otte blev seks fundet at fluorescere under ultraviolet lys (fem vist; C, D, E, F, G), inklusive en forbi
Fluorescerende molekyler afsløret af kvantekemi og maskinlæringOtte forbindelser blev forudsagt at fluorescere ved en ny metode til design af molekyler. Af de otte blev seks fundet at fluorescere under ultraviolet lys (fem vist; C, D, E, F, G), inklusive en forbi -
 Ny indsigt i bakterielle toksinerEscherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH Et toksin produceret af en bakterie, der forårsager urinvejsinfektioner, er relateret til, dog anderledes på vigtige måder fra, gif
Ny indsigt i bakterielle toksinerEscherichia coli. Kredit:Rocky Mountain Laboratories, NIAID, NIH Et toksin produceret af en bakterie, der forårsager urinvejsinfektioner, er relateret til, dog anderledes på vigtige måder fra, gif -
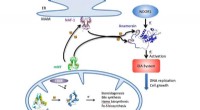 MiNT -protein et nyt mål for at angribe sygdomEn illustration skitserer NEET-cyklussen i celler, hvormed jern-svovlklynger leveres af MiNT, mitoNEET (mNT) og NAF-1 proteiner i cytosolen eller mitokondrierne (bunden) til en række cellulære metabol
MiNT -protein et nyt mål for at angribe sygdomEn illustration skitserer NEET-cyklussen i celler, hvormed jern-svovlklynger leveres af MiNT, mitoNEET (mNT) og NAF-1 proteiner i cytosolen eller mitokondrierne (bunden) til en række cellulære metabol
- NASA-producerede skadekort kan hjælpe Mexico med jordskælvsreaktion
- Borgerforskere opdager et cyklisk kompleksitetsmønster i solstorme
- Har du plettet bakteriecellevæggen eller cytoplasmaet?
- I over 1500 år var den accepterede forklaring på oprindelse og variation af liv på jorden baseret…
- Hvad sker der med den termiske energi fra et objekt, når temperaturen mindsker den øges?
- to fodboldspillere sparker den samme 2-kg bold ad gangen i modsatte retninger. Den ene sparker med e…


