En organisk forbindelse, der ikke er opløselig i vand?
kulbrinter:
* hexan (C6H14): Et almindeligt opløsningsmiddel, der bruges i laboratorier, hexan er et ikke -polært molekyle og blandes således ikke med vand.
* benzen (C6H6): En cyklisk carbonhydrid, benzen er også ikke -polær og uopløselig i vand.
* toluen (C7H8): Et andet almindeligt opløsningsmiddel, toluen, er en ikke -polær væske.
Fedt og olier:
* olivenolie (blanding af triglycerider): Olier er sammensat af lange kæder af fedtsyrer, som er ikke -polære og derfor uopløselige i vand.
* smør (blanding af fedt og vand): Mens smør indeholder noget vand, er flertallet fedt, hvilket gør det mest uopløseligt.
Andre eksempler:
* naphthalen (C10H8): Et fast carbonhydrid, naphthalen er hovedkomponenten i møllekugler.
* chlorobenzen (C6H5CL): Denne forbindelse har en ikke-polær benzenring og en let polær carbon-chlorbinding, hvilket gør den uopløselig i vand.
Hvorfor er disse forbindelser uopløselige i vand?
Den generelle tommelfingerregel er "som opløser som". Vand er et polært molekyle, hvilket betyder, at det har en positiv og negativ ende. Ikke -polære molekyler som kulbrinter har ikke denne adskillelse af ladning og tiltrækkes derfor ikke af vandmolekyler. Denne mangel på tiltrækning forhindrer dem i at opløse.
Fortæl mig, hvis du gerne vil udforske nogen af disse forbindelser mere detaljeret!
Sidste artikelHvad er det kemiske symbol for benzin?
Næste artikelHvordan syntetiseres ketosyrer?
 Varme artikler
Varme artikler
-
 Ny teknik til at identificere kilden til madforgiftningKredit:CC0 Public Domain Forskere ved University of Aberdeen har udviklet en ny teknik, der kan hjælpe med at identificere kilden til madforgiftning eller infektion hurtigere og mere præcist end d
Ny teknik til at identificere kilden til madforgiftningKredit:CC0 Public Domain Forskere ved University of Aberdeen har udviklet en ny teknik, der kan hjælpe med at identificere kilden til madforgiftning eller infektion hurtigere og mere præcist end d -
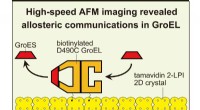 Et chaperonin protein, GroEL, har en mere kompleks mekanisme, end man troede førHS-AFM-billeddannelse afslørede allosterisk interring-kommunikation i GroEL, der styrer dens chaperoninreaktion. For at visualisere dynamiske GroEL-GroES-interaktioner med højhastigheds AFM, GroEL bio
Et chaperonin protein, GroEL, har en mere kompleks mekanisme, end man troede førHS-AFM-billeddannelse afslørede allosterisk interring-kommunikation i GroEL, der styrer dens chaperoninreaktion. For at visualisere dynamiske GroEL-GroES-interaktioner med højhastigheds AFM, GroEL bio -
 Sneeze cam afslører de bedste stofkombinationer til stofmaskerKredit:Pixabay/CC0 Public Domain Under COVID-19-pandemien, Stof ansigtsmasker blev en måde at hjælpe med at beskytte dig selv og andre mod virussen. Og for nogle mennesker, de blev et fashion stat
Sneeze cam afslører de bedste stofkombinationer til stofmaskerKredit:Pixabay/CC0 Public Domain Under COVID-19-pandemien, Stof ansigtsmasker blev en måde at hjælpe med at beskytte dig selv og andre mod virussen. Og for nogle mennesker, de blev et fashion stat -
 Forskere bliver ru med nanomaterialer for at eliminere problematisk klæbrighed forårsaget af glatt…Øverste billede (fra venstre mod højre):Undergraduate Katerina Kimes (siddende), Professor Tevis Jacobs, Bachelorstuderende Cameron Kisailus, og ph.d. Kandidat Abhijeet Gujrati ser på et kort over ove
Forskere bliver ru med nanomaterialer for at eliminere problematisk klæbrighed forårsaget af glatt…Øverste billede (fra venstre mod højre):Undergraduate Katerina Kimes (siddende), Professor Tevis Jacobs, Bachelorstuderende Cameron Kisailus, og ph.d. Kandidat Abhijeet Gujrati ser på et kort over ove
- Hvordan er bevægelsen af partikler i en gas afvige fra væske?
- Europæisk-japansk rummission får det første glimt af Merkur
- Hvor mange kubikmeter i 10000 liter vand?
- Langsigtet satellitanalyse viser regntiden vådere nu end nogensinde
- Hvor skyskraber være energieffektiv?
- Udvides eller samles vand, når det opvarmes?


