Hvad sker der med et molekyle, når det reduceres?
* øget elektrondensitet: Molekylet bliver mere negativt ladet.
* Nedsat oxidationstilstand: Oxidationsnummeret for molekylet falder.
* Ændringer i kemiske egenskaber: Reduktion ændrer ofte molekylets reaktivitet og opførsel. For eksempel kan en reduktion gøre et molekyle mere stabil eller mindre reaktiv.
* Mulig dannelse af nye obligationer: Elektroner opnået under reduktion kan bruges til at danne nye bindinger med andre atomer.
Her er nogle eksempler:
* i organisk kemi: Reduktion kan omdanne en keton til en alkohol, en alkenen til en alkan eller en nitrogruppe til en amin.
* i biologiske systemer: Reduktion er afgørende for mange biologiske processer, såsom respiration og fotosyntesen. I respiration reduceres glukose for eksempel til kuldioxid og frigiver energi.
Vigtig note: Reduktion forekommer altid sammen med oxidation , hvor et andet molekyle mister elektroner. Dette er kendt som en redox -reaktion . Molekylet, der mister elektroner, siges at være oxideret.
Sammenfattende er reduktion processen med at vinde elektroner, hvilket fører til ændringer i et molekyls elektrondensitet, oxidationstilstand, kemiske egenskaber og potentiel bindingsdannelse.
Sidste artikelHvilke organelle pakker og skibe stof ud af cellen?
Næste artikelHvad beskriver bedst en celle, der er isotonisk for stof?
 Varme artikler
Varme artikler
-
 Fremtidens bæredygtige lim klæber ikke fastTeamets næste trin er at finde den bedste applikation til lokalsamfund og industrier, der kan have størst gavn af at bruge klæbemidlet, afbilledet her. Kredit:Boston University For planetens og vo
Fremtidens bæredygtige lim klæber ikke fastTeamets næste trin er at finde den bedste applikation til lokalsamfund og industrier, der kan have størst gavn af at bruge klæbemidlet, afbilledet her. Kredit:Boston University For planetens og vo -
 Forskere udvikler en ny heterostrukturkatalysator til effektiv brintgenerering fra vandspaltningAC Transit brint brændselscelle bus. Kredit:Eric Fischer. Bekymringer om stigende atmosfæriske kuldioxidniveauer og global opvarmning har gjort det til en miljømæssig nødvendighed at erstatte fossi
Forskere udvikler en ny heterostrukturkatalysator til effektiv brintgenerering fra vandspaltningAC Transit brint brændselscelle bus. Kredit:Eric Fischer. Bekymringer om stigende atmosfæriske kuldioxidniveauer og global opvarmning har gjort det til en miljømæssig nødvendighed at erstatte fossi -
 Sikrere, mere komfortable soldatuniformer er i gangI en test, ubehandlet stof (venstre panel) brænder helt efter en flamme er fjernet, der henviser til, at stof, der er behandlet med fytinsyre (højre panel), er selvslukkende på få sekunder efter, at t
Sikrere, mere komfortable soldatuniformer er i gangI en test, ubehandlet stof (venstre panel) brænder helt efter en flamme er fjernet, der henviser til, at stof, der er behandlet med fytinsyre (højre panel), er selvslukkende på få sekunder efter, at t -
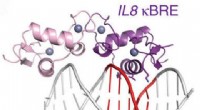 Duel af de inflammatoriske masterregulatorer – indsigt til lægemiddelopdagelseFigur:Diagram over glukokortikoidreceptoren, der binder et NF-kappaB-sted. Kredit:Hudson et al. Naturkommunikation (2018). Anti-inflammatoriske lægemidler såsom dexamethason kan have skadelige biv
Duel af de inflammatoriske masterregulatorer – indsigt til lægemiddelopdagelseFigur:Diagram over glukokortikoidreceptoren, der binder et NF-kappaB-sted. Kredit:Hudson et al. Naturkommunikation (2018). Anti-inflammatoriske lægemidler såsom dexamethason kan have skadelige biv
- Hvordan vi sporede en bemærkelsesværdig flyvning af en lille havfugleart ind i en tyfon
- Hvad er den bedste ligning for kraft?
- Hvor kommer gassen fra det, der går i BIC -tændere?
- Hvad sker der med jordens densitet, når du går fra det ydre lag kerne?
- Nærbilleder viser Saturns ringe i hidtil usete detaljer
- Hvilke planter vokser i ørkenklimaet?


