Hvorfor er phosphoanhydridbindingen mellem phosphatgruppe i ATP omtalt som en høj energiobligation?
1. Termodynamiske overvejelser:
* høj fri energi af hydrolyse: Hydrolysen af phosphoanhydridbindingen frigiver en betydelig mængde fri energi (omkring -30,5 kJ/mol). Dette betyder, at reaktionen er exergonisk, hvilket favoriserer opdelingen af ATP til ADP og uorganisk phosphat (PI). Denne energiudgivelse kan bruges til at drive andre Eandergonic -reaktioner i cellen.
* Resonansstabilisering: Produkterne af ATP -hydrolyse (ADP og PI) er mere stabile end ATP på grund af øget resonansstabilisering. Denne forskel i stabilitet bidrager til den høje frie energi af hydrolyse.
* Elektrostatisk frastødning: De negative ladninger på fosfatgrupperne skaber elektrostatisk frastødning inden for ATP -molekylet. Denne frastødelse er lettet over hydrolyse, hvilket bidrager til energiudgivelsen.
2. Biokemisk funktion:
* Energivaluta: Det høje energiindhold i phosphoanhydridbindingen gør ATP til den primære energifulde i cellen. Det kan bruges til at drive forskellige metaboliske processer, herunder:
* Muskelkontraktion: ATP giver energien til muskelproteiner til at interagere og generere bevægelse.
* Aktiv transport: ATP -kræfter pumper, der bevæger molekyler over cellemembraner mod koncentrationsgradienter.
* biosyntese: ATP tilvejebringer energi til syntese af komplekse molekyler som proteiner, kulhydrater og lipider.
* signaltransduktion: ATP kan bruges til at aktivere signalveje i cellen.
3. Det er en fejlnummer:
Selvom det ofte omtales som en "højenergi-binding", er det vigtigt at præcisere, at phosphoanhydridbindingen faktisk ikke har høj energi. Energien frigøres under bindingens hydrolyse, ikke opbevaret i selve bindingen. Udtrykket "højenergi-binding" er en praktisk korthed for den store mængde energi, der frigives under hydrolyse.
Kortfattet:
Phosphoanhydridbindingen i ATP betragtes som en "højenergi-binding" på grund af dens høje frie energi af hydrolyse, der er drevet af faktorer som resonansstabilisering og elektrostatisk frastødning. Denne energiudgivelse brænder mange essentielle cellulære processer, hvilket gør ATP til den centrale energifaluta i livet.
 Varme artikler
Varme artikler
-
 Fødevarekvalitetskontrol blev gjort hurtigere og lettereBaseret på ultrahøjtydende væskekromatografi-massespektrometri (UHPLC-MS) har videnskabsfolk ved det tekniske universitet i München (TUM) og Leibniz-instituttet for fødevarebiologi udviklet en ny meto
Fødevarekvalitetskontrol blev gjort hurtigere og lettereBaseret på ultrahøjtydende væskekromatografi-massespektrometri (UHPLC-MS) har videnskabsfolk ved det tekniske universitet i München (TUM) og Leibniz-instituttet for fødevarebiologi udviklet en ny meto -
 Undersøgelse finder fluor som mulig erstatning for lithium i genopladelige batterierHer, lagdelte elektroder, såsom Ca2N og Y2C - der har en elektron, der optager et gittersted - forudsiges som lovende værter for fluorid-interkalation, fordi deres anioniske elektroner skaber store me
Undersøgelse finder fluor som mulig erstatning for lithium i genopladelige batterierHer, lagdelte elektroder, såsom Ca2N og Y2C - der har en elektron, der optager et gittersted - forudsiges som lovende værter for fluorid-interkalation, fordi deres anioniske elektroner skaber store me -
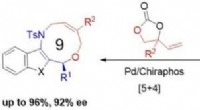 Syntese af mellemstore ringstrukturerede forbindelserFigur viser reaktionsskemaet for kemiske forbindelser med ni- og ti-leddet ringdannelse. Chiraphos og SIPHOX er to kommercielt tilgængelige forbindelser. Kredit:National University of Singapore NU
Syntese af mellemstore ringstrukturerede forbindelserFigur viser reaktionsskemaet for kemiske forbindelser med ni- og ti-leddet ringdannelse. Chiraphos og SIPHOX er to kommercielt tilgængelige forbindelser. Kredit:National University of Singapore NU -
 Undersøgelse viser, at keramik kan deformere som metaller, hvis det sintres under et elektrisk feltPurdue-forskere observerede for første gang, hvordan keramik dannet under et elektrisk felt overraskende ændrer form i stedet for at gå i stykker, når det komprimeres ved høj belastning. På billedet:U
Undersøgelse viser, at keramik kan deformere som metaller, hvis det sintres under et elektrisk feltPurdue-forskere observerede for første gang, hvordan keramik dannet under et elektrisk felt overraskende ændrer form i stedet for at gå i stykker, når det komprimeres ved høj belastning. På billedet:U
- Alaska-skælvet viser kompleksiteten af tsunami-advarsler
- Arbejdsglæden falder med digitaliseringen
- Hvordan er magt relateret til magt?
- Bestem antallet af bindingselektroner og ikke -bonding i struktur CO2?
- Udtalelse:Det er tid til at kræve ejerskab af vores digitale liv
- En simpel eftermontering omdanner elektronmikroskoper til højhastighedskameraer i atomskala


