Hvorfor er tilstødende vandmolekyler forbundet med?
Her er hvorfor:
* Polaritet: Vandmolekyler er polære, hvilket betyder, at de har en lidt positiv ende (nær brintatomerne) og en lidt negativ ende (nær iltatomet). Dette skyldes den ujævne deling af elektroner mellem ilt og brint.
* attraktion: Den positive ende af et vandmolekyle tiltrækkes af den negative ende af et andet vandmolekyle. Denne attraktion kaldes A hydrogenbinding .
* svag, men mange: Mens individuelle brintbindinger er relativt svage, er der mange af dem i flydende vand. Dette skaber en stærk samlet attraktion mellem vandmolekyler, som er ansvarlig for vandets unikke egenskaber.
Disse brintbindinger er det, der giver vand sit høje kogepunkt, overfladespænding og evne til at opløse mange stoffer.
Sidste artikelHvordan ser molekylerne af C3H7O2N ud?
Næste artikelEr ilt produceret af den lysafhængige reaktion?
 Varme artikler
Varme artikler
-
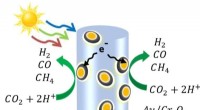 Soldrevet kemi bruger kuldioxid og vand til at fremstille råmaterialer til brændstoffer, kemikalie…Et diagram over halvledernannotrådene lavet af indium, gallium og nitrogen - dekoreret med guld- og kromoxidnanopartikler. Når lyset rammer nanotråden, frigør det elektroner og de positivt ladede hull
Soldrevet kemi bruger kuldioxid og vand til at fremstille råmaterialer til brændstoffer, kemikalie…Et diagram over halvledernannotrådene lavet af indium, gallium og nitrogen - dekoreret med guld- og kromoxidnanopartikler. Når lyset rammer nanotråden, frigør det elektroner og de positivt ladede hull -
 Struktur af den molekylære maskine, der forbinder kulhydrat- og lipidmetabolismeKredit:CC0 Public Domain Et forskerhold ledet af Dr. Kenneth Verstraete i Enheden for Strukturel Biologi ved VIB-UGent Center for Inflammationsforskning har afsløret den tredimensionelle struktur
Struktur af den molekylære maskine, der forbinder kulhydrat- og lipidmetabolismeKredit:CC0 Public Domain Et forskerhold ledet af Dr. Kenneth Verstraete i Enheden for Strukturel Biologi ved VIB-UGent Center for Inflammationsforskning har afsløret den tredimensionelle struktur -
 Forskere udvikler ny teknologi, der kan fremskynde kommercialiseringen af brændselscellekøretøj…Et hold af UD-ingeniørfakultetets medlemmer og afdelingsledere samlede deres forskningsgrupper til en brændselscelle-innovation. Denne illustration inkluderer professorerne Ajay K. Prasad, Suresh G. A
Forskere udvikler ny teknologi, der kan fremskynde kommercialiseringen af brændselscellekøretøj…Et hold af UD-ingeniørfakultetets medlemmer og afdelingsledere samlede deres forskningsgrupper til en brændselscelle-innovation. Denne illustration inkluderer professorerne Ajay K. Prasad, Suresh G. A -
 Bedre vurdering af bakteriers følsomhed over for antibiotika kan ændre, hvordan lægemidler ordine…En mikrochip-antibiotisk testplatform, der reducerer den nødvendige tid til at identificere den rigtige medicin, udviklet af forskere ved Korea Advanced Institute of Science and Technology. Kredit:Jeo
Bedre vurdering af bakteriers følsomhed over for antibiotika kan ændre, hvordan lægemidler ordine…En mikrochip-antibiotisk testplatform, der reducerer den nødvendige tid til at identificere den rigtige medicin, udviklet af forskere ved Korea Advanced Institute of Science and Technology. Kredit:Jeo
- Videnskab har magt til at øge landbruget i Afrika - men meget skal ændres
- Hvad er biproduktet af saccharose?
- Kan videnskab bedømme, hvad er eller ikke en moralsk acceptabel anvendelse af bioteknologi?
- Kontrolleret frigivelse af gødning ved hjælp af biopolymerspåner
- Højhastighedsforsøg viser, hvad der sker, når polymervæsker revner
- Amøbe-inspireret computersystem overgår konventionelle optimeringsmetoder


