Forståelse af atomreaktivitet:Elektronernes rolle
* Valenselektroner: Disse er elektronerne i det yderste energiniveau af et atom. Det er dem, der er involveret i kemisk binding.
* Elektronkonfiguration: Dette beskriver, hvordan elektroner er fordelt inden for et atoms forskellige energiniveauer og orbitaler.
Sådan påvirker disse faktorer reaktivitet:
* Atomer har tendens til at opnå stabilitet: Atomer er mest stabile, når deres yderste skal (valensskal) er fuld. Dette opnås ofte ved at vinde, miste eller dele elektroner for at ligne elektronkonfigurationen af en ædelgas, som har fuld valensskaller og er meget ureaktive.
* Elektronegativitet: Dette er et mål for et atoms evne til at tiltrække elektroner i en kemisk binding. Atomer med høj elektronegativitet har tendens til at få elektroner, mens atomer med lav elektronegativitet har tendens til at miste elektroner.
* Ioniseringsenergi: Dette er den energi, der kræves for at fjerne en elektron fra et atom. Atomer med lav ioniseringsenergi mister let elektroner, mens dem med høj ioniseringsenergi holder tæt på deres elektroner.
Opsummering: Et atoms reaktivitet er dikteret af dets ønske om at opnå en stabil elektronkonfiguration, som er påvirket af antallet af valenselektroner og atomets elektronegativitet og ioniseringsenergi.
Sig til, hvis du vil have en mere detaljeret forklaring på nogen af disse faktorer!
 Varme artikler
Varme artikler
-
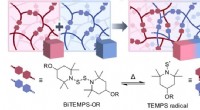 Blanding af det ublandbare:En ny tilgang til effektiv sammensmeltning af forskellige polymerer80°C. Efter afkøling, TEMPS-radikalerne slutter sig igen, muliggør fusion af forskellige tværbundne polymerer. Kredit: Angewandte Chemie Tværbundne polymerer er strukturer, hvor store molekylære
Blanding af det ublandbare:En ny tilgang til effektiv sammensmeltning af forskellige polymerer80°C. Efter afkøling, TEMPS-radikalerne slutter sig igen, muliggør fusion af forskellige tværbundne polymerer. Kredit: Angewandte Chemie Tværbundne polymerer er strukturer, hvor store molekylære -
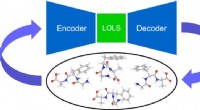 Ny maskinlæringstilgang letter molekylær konformersøgning i komplekse molekylerKredit:Aalto Universitet CEST-forskere udviklede en ny maskinlæringstilgang baseret på et lav-energi latent rum (LOLS) og densitets funktionel teori (DFT) til at søge efter molekylære konformere.
Ny maskinlæringstilgang letter molekylær konformersøgning i komplekse molekylerKredit:Aalto Universitet CEST-forskere udviklede en ny maskinlæringstilgang baseret på et lav-energi latent rum (LOLS) og densitets funktionel teori (DFT) til at søge efter molekylære konformere. -
 Bioingeniører udvikler 3-D strukturer fra krabbeskaller til at erstatte beskadiget vævEt 3D-stillads efter laserstereolitografi (a) og lyofilisering (b). Kredit:Ksenia Bardakova Et team af forskere fra Sechenov First Moscow State Medical University brugte 3-D-print til at skabe bio
Bioingeniører udvikler 3-D strukturer fra krabbeskaller til at erstatte beskadiget vævEt 3D-stillads efter laserstereolitografi (a) og lyofilisering (b). Kredit:Ksenia Bardakova Et team af forskere fra Sechenov First Moscow State Medical University brugte 3-D-print til at skabe bio -
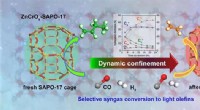 Dynamisk indeslutning af SAPO-17-bure på selektivitetskontrol af syngaskonverteringDynamisk indeslutning af SAPO-17-bure på selektivitetskontrol af syngaskonvertering. Kredit:Wang Haodi og Jiao Feng Et forskerhold ledet af prof. Pan Xiulian og prof. Bao Xinhe fra Dalian Institute
Dynamisk indeslutning af SAPO-17-bure på selektivitetskontrol af syngaskonverteringDynamisk indeslutning af SAPO-17-bure på selektivitetskontrol af syngaskonvertering. Kredit:Wang Haodi og Jiao Feng Et forskerhold ledet af prof. Pan Xiulian og prof. Bao Xinhe fra Dalian Institute
- En kvante -centrifugeringsvæske:Honeycomb -gitter opfylder undvigende standarder for Kitaev -modell…
- Vejr alle klipper på samme måde?
- Hvad beskriver loven om bevaringsenergi?
- Kan solar geoengineering afbøde både klimaændringer og indkomstulighed?
- Forbedret model for massefordelingen af galaksehoben SMACS J0723.3−7327 baseret på Webb-teleskopb…
- 100 ml 0,200 moll NaCl blandes med 400 ml Hvad koncentrations Cl i den resulterende opløsning?


