Isotoniske løsninger:Identifikation og måling
Sådan kan du identificere, om to løsninger er isotoniske:
1. Direkte måling af osmotisk tryk:
* Denne metode involverer brug af et osmometer, en enhed, der måler det tryk, der kræves for at forhindre, at vand strømmer hen over en semipermeabel membran.
* Hvis det osmotiske tryk af de to opløsninger er det samme, er de isotoniske.
2. Sammenligning af koncentrationen af opløste stoffer:
* For ikke-elektrolytløsninger: Hvis koncentrationen af opløste stoffer (med hensyn til molaritet eller molalitet) er den samme i begge opløsninger, er de isotoniske.
* Til elektrolytopløsninger: Du skal tage højde for dissociationen af elektrolytter. For eksempel vil en 1 M opløsning af NaCl have det dobbelte osmotiske tryk af en 1 M opløsning af glukose, fordi NaCl dissocierer i to ioner (Na+ og Cl-).
* Beregning af effektiv osmolaritet: For at sammenligne elektrolytopløsninger skal du beregne den effektive osmolaritet, som tager hensyn til antallet af partikler produceret ved dissociation. For eksempel:
* 1 M NaCl-opløsning har en osmolaritet på 2 Osm (1 M Na+ + 1 M Cl-)
* 1 M glucoseopløsning har en osmolaritet på 1 Osm (1 M glucose)
* Hvis den effektive osmolaritet er den samme for begge opløsninger, er de isotoniske.
3. Observation af celleadfærd:
* Forsøg med røde blodlegemer: Placer røde blodlegemer i hver af opløsningerne.
* Hvis cellerne forbliver uændrede, er opløsningerne isotoniske.
* Hvis cellerne skrumper, er opløsningen hypertonisk (højere koncentration af opløst stof).
* Hvis cellerne svulmer eller brister, er opløsningen hypotonisk (lavere koncentration af opløst stof).
Vigtige overvejelser:
* Temperatur: Osmotisk tryk påvirkes af temperaturen. Sørg for, at begge opløsninger har samme temperatur, når du sammenligner dem.
* Membrantype: Permeabiliteten af den semipermeable membran kan også påvirke vandets bevægelse. Sørg for, at du bruger den samme type membran til dit eksperiment.
For at afgøre, om to opløsninger er isotoniske, kan du kort sagt enten måle deres osmotiske tryk direkte, sammenligne koncentrationen af opløste stoffer (der står for dissociation) eller observere opførselen af celler placeret i hver opløsning.
 Varme artikler
Varme artikler
-
 Forskere finder ud af, at vanddråber kan omdannes til hydrogenperoxid, når de kondenserer på kold…Billedet viser vandmikrodråber-kondensat dannet på overfladen af en glasbeholder indeholdende koldt vand (til venstre) og et billede af vanddråber dannet på en poleret siliciumoverflade (til højre).
Forskere finder ud af, at vanddråber kan omdannes til hydrogenperoxid, når de kondenserer på kold…Billedet viser vandmikrodråber-kondensat dannet på overfladen af en glasbeholder indeholdende koldt vand (til venstre) og et billede af vanddråber dannet på en poleret siliciumoverflade (til højre). -
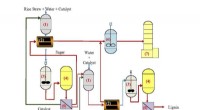 Forskere tager to skridt mod grønt brændstofForskere designet to-trins proces til at nedbryde risstrå til sukker til brændstof. Kredit:Figur tilpasset fra Ind. Eng. Chem. Res. 2019 58 (14), 5686-5697. © 2019 American Chemical Society Et i
Forskere tager to skridt mod grønt brændstofForskere designet to-trins proces til at nedbryde risstrå til sukker til brændstof. Kredit:Figur tilpasset fra Ind. Eng. Chem. Res. 2019 58 (14), 5686-5697. © 2019 American Chemical Society Et i -
 Forskere kommer op med en hurtigere måde at opdage antibiotika påKredit:Elena Khavina/MIPT Pressekontor Russiske biokemikere har identificeret en lovende ny klasse af antibiotika. Efter at have studeret over 125, 000 molekyler, de fandt, at 2-pyrazol-1-yl-thiaz
Forskere kommer op med en hurtigere måde at opdage antibiotika påKredit:Elena Khavina/MIPT Pressekontor Russiske biokemikere har identificeret en lovende ny klasse af antibiotika. Efter at have studeret over 125, 000 molekyler, de fandt, at 2-pyrazol-1-yl-thiaz -
 Tidlig advarselssensor opsnuser skadelig gas i byerKredit: ACS sensorer (2020). DOI:10.1021/acssensors.9b02318 En integreret detektorenhed kunne danne grundlag for et distribueret luftkvalitetssensornetværk. Designet til en elektronisk sensor, d
Tidlig advarselssensor opsnuser skadelig gas i byerKredit: ACS sensorer (2020). DOI:10.1021/acssensors.9b02318 En integreret detektorenhed kunne danne grundlag for et distribueret luftkvalitetssensornetværk. Designet til en elektronisk sensor, d
- Robotter, der roamer i antarktiske farvande, afslører, hvorfor Ross Ice Shelf smelter hurtigt om so…
- Er det sandt eller falskt, at celleteori-cellerne er produceret fra ikke-levende celler?
- Hvorfor holder Nucler Fusion løfte som en energikilde?
- Hvad er massenummeret på et bromatom?
- Hvad sker der, når du blander platinoxygen og svovldioxid?
- Hvor mange galakser er der i dit solsystem?


