Grahams lov om effusion:Gasdiffusionshastigheder og molmasse
Forstå Grahams lov
Grahams lov siger, at hastigheden af udstrømning af en gas er omvendt proportional med kvadratroden af dens molære masse. I enklere vendinger, lettere gasser strømmer ud (eller diffunderer) hurtigere end tungere gasser.
Formlen
Formlen for Grahams lov er:
Rate₁ / Rate₂ =√(M₂ / M₁)
Hvor:
* Rate₁ er udstrømningshastigheden af gas 1
* Rate₂ er hastigheden af udstrømning af gas 2
* M 1 er den molære masse af gas 1
* M₂ er den molære masse af gas 2
Løsning af problemet
1. Identificer de kendte:
* Rate₁ (ukendt gas) =1 (vi antager, at det er 1, da det diffunderer langsommere)
* Rate2 (H2) =2,92
* M2 (H2) =2,016 g/mol
2. Opsæt ligningen:
1/2,92 =√(2,016 g/mol/M₁)
3. Løs for M₁ (molmassen af den ukendte gas):
* (1/2,92)2 =2,016 g/mol/M1
* M1 =2,016 g/mol/(1/2,92)2
* M1 ≈ 17,0 g/mol
Derfor er molmassen af den ukendte gas ca. 17,0 g/mol.
Vigtig bemærkning: Dette forudsætter, at den ukendte gas opfører sig ideelt, og at temperaturen og trykket er konstant.
Sidste artikelNAD+-genbrug i anaerob metabolisme:Forståelse af processen
Næste artikelForståelse af triglycerider:struktur og sammensætning
 Varme artikler
Varme artikler
-
 Forskere finder potentiel anvendelse for genbrugsplast i betonFra venstre, ingeniørfakultetet Adrienne Phillips, Cecily Ryan og Chelsea Heveran, sammen med doktorgradsstuderende Seth Kane og senior Michael Espinal viser prøver i deres laboratorium relateret til
Forskere finder potentiel anvendelse for genbrugsplast i betonFra venstre, ingeniørfakultetet Adrienne Phillips, Cecily Ryan og Chelsea Heveran, sammen med doktorgradsstuderende Seth Kane og senior Michael Espinal viser prøver i deres laboratorium relateret til -
 Instant messaging i proteiner opdagetLisa-Marie Funk, medførsteforfatter, analysere proteinkrystaller ved hjælp af et mikroskop forud for besøget i DESY Hamburg. Kredit:Nora Eulig Proteiner er essentielle for enhver levende celle og
Instant messaging i proteiner opdagetLisa-Marie Funk, medførsteforfatter, analysere proteinkrystaller ved hjælp af et mikroskop forud for besøget i DESY Hamburg. Kredit:Nora Eulig Proteiner er essentielle for enhver levende celle og -
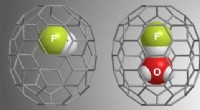 Forskere isolerer hydrogenfluorid og vand for at forstå syreopløsningKredit:Zhang et al. (Phys.org)—Kemiundervisning på begynderniveau lærer om Brønsted-Lowry-syrer. Disse syrer dissocierer i vand og danner et H + ion og en negativt ladet modion. Selvom dette er
Forskere isolerer hydrogenfluorid og vand for at forstå syreopløsningKredit:Zhang et al. (Phys.org)—Kemiundervisning på begynderniveau lærer om Brønsted-Lowry-syrer. Disse syrer dissocierer i vand og danner et H + ion og en negativt ladet modion. Selvom dette er -
 Forskere øger varmen på smeltede metaller for at skabe fremtidige teknologierBryan Owens-Baird, en kandidatstuderende forsker fra Iowa State University, forbereder sig på at studere en af sine prøver, en pulveriseret forbindelse af fosfor, silicium, og tin, med NOMAD -instru
Forskere øger varmen på smeltede metaller for at skabe fremtidige teknologierBryan Owens-Baird, en kandidatstuderende forsker fra Iowa State University, forbereder sig på at studere en af sine prøver, en pulveriseret forbindelse af fosfor, silicium, og tin, med NOMAD -instru
- Sådan laver du en perfekt solfanger
- I hvilken type stjerneklynge er stjernerne grupperet sammen i en løs formation med bred variation m…
- Hvilken branche bruger elektromagneter?
- Olga Tokarczuk, Peter Handke vinder Nobels litteraturpriser
- Virtuelle test for autonome køresystemer
- En organisk væske nedbrydes ved 80 graders celsius. Dens dampbesætning, at temperaturen er 36 mmHg…


