Identifikation af det begrænsende reagens i kemiske reaktioner:En omfattende vejledning
Sådan bestemmes det begrænsende reagens:
1. Skriv en afbalanceret kemisk ligning: Dette viser de støkiometriske forhold mellem reaktanter og produkter.
2. Beregn antallet af mol af hver reaktant: Brug de givne masser og molære masser.
3. Bestem molforholdet mellem reaktanter: Sammenlign de beregnede mol af hver reaktant med de støkiometriske koefficienter i den afbalancerede ligning.
4. Identificer det begrænsende reagens: Reaktanten med det mindste molforhold i forhold til dens koefficient i den afbalancerede ligning er det begrænsende reagens.
Eksempel:
Overvej reaktionen:
2 H2 (g) + O2 (g) → 2 H2O (l)
Lad os sige, at vi har:
* 4 gram H₂
* 16 gram O₂
1. Balanceret ligning: Allerede givet.
2. Moler reaktanter:
* H2:4 g / 2 g/mol =2 mol
* O2:16 g / 32 g/mol =0,5 mol
3. Molforhold:
* H2:2 mol / 2 =1
* O2:0,5 mol/1 =0,5
4. Begrænsende reagens: O₂ har det mindre molforhold (0,5) sammenlignet med dets koefficient i den balancerede ligning (1). Derfor er O₂ det begrænsende reagens .
Vigtig bemærkning: Det begrænsende reagens bestemmer det teoretiske udbytte af produktet, som er den maksimale mængde produkt, der kan dannes.
 Varme artikler
Varme artikler
-
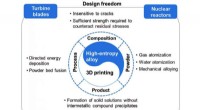 Forskere gennemgår fremskridt inden for 3D-print af højentropi-legeringerOversigt over forholdet mellem HEAer og 3D-print, med hensyn til kompositionsdesignet, pulver udvikling, trykprocesser, produkt egenskaber, og potentielle applikationer. Kredit:SUTD Højentropi-leg
Forskere gennemgår fremskridt inden for 3D-print af højentropi-legeringerOversigt over forholdet mellem HEAer og 3D-print, med hensyn til kompositionsdesignet, pulver udvikling, trykprocesser, produkt egenskaber, og potentielle applikationer. Kredit:SUTD Højentropi-leg -
 Forskere udvikler ny metode til at analysere metalHærens forskere Dr. Stephen Berkebile (til venstre) og Nikhil Murthy (til højre) undersøger, hvordan siliciumnitrid reagerer på stål under tør glidende mekanisk kontakt for bedre at forstå udstyrsnedb
Forskere udvikler ny metode til at analysere metalHærens forskere Dr. Stephen Berkebile (til venstre) og Nikhil Murthy (til højre) undersøger, hvordan siliciumnitrid reagerer på stål under tør glidende mekanisk kontakt for bedre at forstå udstyrsnedb -
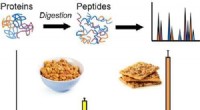 Fanger af rugmetoden opdager rugglutenproteiner i fødevarerKredit:American Chemical Society Glutenfri diæter har været trendy i flere år nu, med tilhængere, der hævder, at undgå korn, der indeholder stoffet, hjælper med vægttab eller forbedrer det generel
Fanger af rugmetoden opdager rugglutenproteiner i fødevarerKredit:American Chemical Society Glutenfri diæter har været trendy i flere år nu, med tilhængere, der hævder, at undgå korn, der indeholder stoffet, hjælper med vægttab eller forbedrer det generel -
 Forskere rapporterer kraftig ionoverførsel i ladet vdW-klynge for første gangSammenfaldskortet viser tidspunktet for flyvninger mellem det første og det andet fragmention, der ankommer til detektoren. Kredit:IMP Siden opdagelsen af den dobbelte helixform af DNA og hypote
Forskere rapporterer kraftig ionoverførsel i ladet vdW-klynge for første gangSammenfaldskortet viser tidspunktet for flyvninger mellem det første og det andet fragmention, der ankommer til detektoren. Kredit:IMP Siden opdagelsen af den dobbelte helixform af DNA og hypote


