Beregning af endelig kloridionkoncentration:En trin-for-trin guide
1. Beregn mol af Cl- fra NaCl:
* 10 mM NaCl =10 mmol/L NaCl
* 1 ml =0,001 L
* Mol NaCl =(10 mmol/L) * (0,001 L) =0,01 mmol NaCl
* Da NaCl opløses i en Na+ og en Cl-, er der også 0,01 mmol Cl- fra NaCl-opløsningen.
2. Beregn mol af Cl- fra CaCl2:
* 0,05 M CaCl2 =0,05 mol/L CaCl2
* 4 ml =0,004 L
* Mol CaCl2 =(0,05 mol/L) * (0,004 L) =0,0002 mol CaCl2
* Da CaCl2 dissocierer i én Ca2+ og to Cl-, er der (0,0002 mol CaCl2) * (2 mol Cl-/mol CaCl2) =0,0004 mol Cl- fra CaCl2-opløsningen.
3. Beregn det samlede antal mol af Cl-:
* Total mol Cl- =0,01 mmol + 0,0004 mol =0,0104 mol Cl-
4. Beregn den endelige koncentration af Cl-:
* Slutvolumen =1 mL + 4 mL =5 mL =0,005 L
* Slutkoncentration af Cl- =(0,0104 mol) / (0,005 L) =2,08 M
Derfor er den endelige koncentration af Cl- 2,08 M.
Sidste artikelAromatiske forbindelser:Udforskning af benzenringkemi
Næste artikelJernholdige metaller:fordele, ulemper og anvendelser
 Varme artikler
Varme artikler
-
 Nyt materiale udsender hvidt lys, når det udsættes for elektricitetElektrisk-stimuli-responsive porøse kulstof-nanoreringer med jod. En elektrisk stimulus inducerer kulbrinte-nanoring cycloparaphenylen (CPP)-iod-samlingen til at vise elektronisk ledningsevne og hvidt
Nyt materiale udsender hvidt lys, når det udsættes for elektricitetElektrisk-stimuli-responsive porøse kulstof-nanoreringer med jod. En elektrisk stimulus inducerer kulbrinte-nanoring cycloparaphenylen (CPP)-iod-samlingen til at vise elektronisk ledningsevne og hvidt -
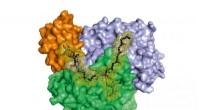 Hvordan opbygger bakterier naturlige produkter?Et kompleks af tre proteiner beskytter det meget reaktive hexaketid, når det forlænges til octaketidet. I samarbejde med andre proteiner, vigtige naturlige stoffer produceres fra det resulterende octa
Hvordan opbygger bakterier naturlige produkter?Et kompleks af tre proteiner beskytter det meget reaktive hexaketid, når det forlænges til octaketidet. I samarbejde med andre proteiner, vigtige naturlige stoffer produceres fra det resulterende octa -
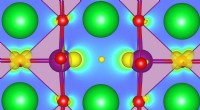 Forskere forbedrer beskrivelsen af defekte oxider med beregning af første principperAt forstå, hvordan defekter kan påvirke grundtilstandsegenskaber, fremme faseovergange, eller muliggøre helt nye funktionaliteter i nogle stærkt korrelerede oxider er blevet et emne af stor interesse
Forskere forbedrer beskrivelsen af defekte oxider med beregning af første principperAt forstå, hvordan defekter kan påvirke grundtilstandsegenskaber, fremme faseovergange, eller muliggøre helt nye funktionaliteter i nogle stærkt korrelerede oxider er blevet et emne af stor interesse -
 Ny struktur af nøgleprotein rummer spor for bedre lægemiddeldesignProber (vist glødende her) afslørede den indre arkitektur af proteinet A2aAR i den nye undersøgelse. Kredit:Kurt Wuthrich og Matthew Eddy, Scripps Research Institute Forskere ved The Scripps Resea
Ny struktur af nøgleprotein rummer spor for bedre lægemiddeldesignProber (vist glødende her) afslørede den indre arkitektur af proteinet A2aAR i den nye undersøgelse. Kredit:Kurt Wuthrich og Matthew Eddy, Scripps Research Institute Forskere ved The Scripps Resea
- Hvad er en groft folieret klippe med båndet udseende kaldet?
- Røgsæsoner er ikke nye, men vores bestræbelser på at kontrollere skovbrande er, og burde ændre …
- Hvilke egenskaber skal en sandstorm betragtes som sandstorm?
- Hvordan husjagtmyrer vælger det bedste hjem
- Hvad kan en videnskabsmand gøre som en del af den videnskabelige proces?
- Forskere udvikler en ny måde at måle væske-sten interaktion i oliereservoir


