Meget reaktive metaller:En omfattende vejledning
Metaller mere reaktive end hydrogen:
* Gruppe 1 (alkalimetaller): Lithium (Li), Natrium (Na), Kalium (K), Rubidium (Rb), Cæsium (Cs), Francium (Fr)
* Gruppe 2 (jordalkalimetaller): Beryllium (Be), Magnesium (Mg), Calcium (Ca), Strontium (Sr), Barium (Ba), Radium (Ra)
* Aluminium (Al)
* Zink (Zn)
* Jern (Fe)
* Tin (Sn)
* Lead (Pb)
Hvorfor er de mere reaktive?
Et metals reaktivitet er relateret til dets tendens til at miste elektroner og danne positive ioner. Metaller, der er mere reaktive end brint, har en stærkere tendens til at miste elektroner og danne positive ioner sammenlignet med brint.
Eksempel:
Når et metal som zink reagerer med saltsyre (HCl), mister zinkatomerne elektroner og danner zinkioner (Zn²⁺), mens hydrogenioner (H⁺) får elektroner og danner brintgas (H₂):
Zn(s) + 2HCl(aq) → ZnCl2(aq) + H2(g)
Bemærk:
* Ædelmetaller (f.eks. guld, sølv, platin) er mindre reaktive end brint og reagerer ikke med syrer.
* Metallers reaktivitet stiger generelt, når du bevæger dig ned ad en gruppe i det periodiske system og falder, når du bevæger dig hen over en periode.
* Denne reaktivitetsserie hjælper med at forudsige resultatet af reaktioner mellem metaller og syrer.
 Varme artikler
Varme artikler
-
 Heliumioner åbner en helt ny verden af materialerKredit:Queensland University of Technology QUT-forskere har fundet en spændende ny måde at manipulere og designe fremtidens materialer på atomniveau og ændre den måde, de opfører sig på i større s
Heliumioner åbner en helt ny verden af materialerKredit:Queensland University of Technology QUT-forskere har fundet en spændende ny måde at manipulere og designe fremtidens materialer på atomniveau og ændre den måde, de opfører sig på i større s -
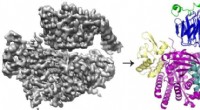 Undersøgelse afslører den indviklede måde, hvorpå to proteiner interagerer for at fremme cellebe…Cryo-EM 3D-rekonstruktionen (til venstre) af proteinet P-Rex1 bundet til Gβγ og proteinmodellen (til højre), der viser, at Gβγ (øverst; blå og grøn) binder til en kompakt, multi-domæne overflade på P-
Undersøgelse afslører den indviklede måde, hvorpå to proteiner interagerer for at fremme cellebe…Cryo-EM 3D-rekonstruktionen (til venstre) af proteinet P-Rex1 bundet til Gβγ og proteinmodellen (til højre), der viser, at Gβγ (øverst; blå og grøn) binder til en kompakt, multi-domæne overflade på P- -
 Producerer brint ved at bruge mindre energiDr. Laith Almazahreh undersøger mekanismen for elektrokatalytisk brintdannelse med en naturinspireret modelforbindelse ved Friedrich Schiller University Jena. Den elektrokemiske celle indeholder en op
Producerer brint ved at bruge mindre energiDr. Laith Almazahreh undersøger mekanismen for elektrokatalytisk brintdannelse med en naturinspireret modelforbindelse ved Friedrich Schiller University Jena. Den elektrokemiske celle indeholder en op -
 Forståelse af kemiske faresymboler:OSHA &NFPA retningslinjerAf Brett Smith, Opdateret 30. august 2022 I USA er kemiske advarselssymboler primært styret af to organisationer:Occupational Safety and Health Administration (OSHA) og non-profit National Fire Prote
Forståelse af kemiske faresymboler:OSHA &NFPA retningslinjerAf Brett Smith, Opdateret 30. august 2022 I USA er kemiske advarselssymboler primært styret af to organisationer:Occupational Safety and Health Administration (OSHA) og non-profit National Fire Prote
- Ældste australske menneske vendte tilbage til 42, 000 år gammel grav
- Hvad former tarmmikrobiomer af Alaskas brune bjørne? Beliggenhed, beliggenhed, beliggenhed
- Sådan finder du vinklerne på en højre trekant
- Hvad er fingeraftryk? | HowStuffWorks
- Restriktioner på ansøgninger om forskningsbevillinger skaber kaos
- Hvor godt match er det? Lægger statistik ind i retsmedicinsk skydevåbenidentifikation


