Forståelse af molekylær polaritet:VSEPR-teori og elektronegativitet
Forstå polaritet
* Polaritet opstår fra ujævn deling af elektroner i en kovalent binding. Dette sker, når det ene atom i bindingen har en højere elektronegativitet (tendens til at tiltrække elektroner) end det andet.
* Dipolmoment: Et molekyle betragtes som polært, hvis det har et netto dipolmoment, hvilket betyder, at der er en adskillelse af positiv og negativ ladning.
* VSEPR (Valence Shell Electron Pair Repulsion) Teori: Denne teori hjælper med at forudsige formen af et molekyle baseret på arrangementet af elektronpar omkring det centrale atom.
Faktorer, der påvirker polaritet:
* Elektronegativitetsforskel: Jo større elektronegativitetsforskel mellem atomer i en binding, jo mere polær er bindingen.
* Molekylær geometri: Selvom individuelle bindinger er polære, kan molekylet være upolært, hvis bindingsdipolerne ophæver hinanden på grund af symmetrisk geometri.
VSEPR-formler og polaritet
Her er hvordan VSEPR-formler kan hjælpe os med at forudsige det mest polære molekyle:
1. Identificer molekyler med meget polære bindinger: Se efter molekyler med store elektronegativitetsforskelle mellem det centrale atom og dets omgivende atomer. Eksempler:
* H-F: Fluor er meget elektronegativt.
* H-Cl: Klor er elektronegativt.
* ÅH: Ilt er elektronegativt.
2. Overvej molekylær geometri:
* Lineær: Lineære molekyler (AX2) er ofte polære, hvis bindingerne er polære. Eksempler:HF, HCl.
* Bøjet: Bøjede molekyler (AX2E) er generelt polære på grund af den ujævne fordeling af elektronpar. Eksempler:H2O, SO2.
* Trigonal pyramideformet: Trigonale pyramideformede molekyler (AX3E) er polære, fordi det centrale atom er omgivet af tre polære bindinger og et ensomt par. Eksempel:NH3.
* Tetrahedral: Tetraedriske molekyler (AX4) kan være polære eller upolære afhængigt af de involverede atomer. Hvis alle omgivende atomer er ens, kan de være upolære (f.eks. CH4). Men hvis der er forskellige atomer, er molekylet normalt polært (f.eks. CHCl3).
Eksempel:
* Vand (H2O):
* VSEPR formel:AX2E2 (bøjet)
* To H-O-bindinger er meget polære.
* Den bøjede geometri forhindrer bindingsdipolerne i at annullere, hvilket resulterer i et netto dipolmoment, hvilket gør det til et meget polært molekyle.
Vigtig bemærkning:
* Mens VSEPR-formler giver os et godt udgangspunkt, skal du henvise til elektronegativitetsværdier og overveje de specifikke atomer, der er involveret for endeligt at bestemme det mest polære molekyle.
Lad mig vide, hvis du har specifikke molekyler i tankerne, så kan jeg hjælpe dig med at analysere deres polaritet.
 Varme artikler
Varme artikler
-
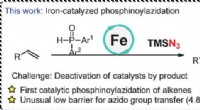 PcFe-katalyseret radikal phosphinoylazidering af alkener med et hurtigt azido-overførselstrinKredit:Dalian Institute of Chemical Physics, Det kinesiske akademis videnskaber Phosphinoylazidation af alkener er en direkte metode til at opbygge nitrogen- og fosforholdige forbindelser fra råst
PcFe-katalyseret radikal phosphinoylazidering af alkener med et hurtigt azido-overførselstrinKredit:Dalian Institute of Chemical Physics, Det kinesiske akademis videnskaber Phosphinoylazidation af alkener er en direkte metode til at opbygge nitrogen- og fosforholdige forbindelser fra råst -
 Udbredt database med molekylære fingeraftryk opgraderetPå dette billede fra 1948, en NIST-forsker driver et tidligt massespektrometer. Kredit:NIST Når videnskabsmænd skal identificere en ukendt forbindelse, de gør, hvad en politidetektiv kan gøre. De
Udbredt database med molekylære fingeraftryk opgraderetPå dette billede fra 1948, en NIST-forsker driver et tidligt massespektrometer. Kredit:NIST Når videnskabsmænd skal identificere en ukendt forbindelse, de gør, hvad en politidetektiv kan gøre. De -
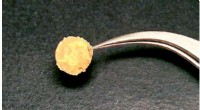 Ny teknik bygger superhårde metaller fra nanopartiklerDenne guldmønt blev lavet af byggesten i nanopartikler, takket være en ny teknik udviklet af Brown University -forskere. Fremstilling af bulkmetaller på denne måde muliggør præcis metalets mikrostrukt
Ny teknik bygger superhårde metaller fra nanopartiklerDenne guldmønt blev lavet af byggesten i nanopartikler, takket være en ny teknik udviklet af Brown University -forskere. Fremstilling af bulkmetaller på denne måde muliggør præcis metalets mikrostrukt -
 Håndtering af jern- og zinkmangel med bedre brødKredit:CC0 Public Domain Sundhedsmæssige virkninger af zink- og jernmangel kan være ødelæggende, især i udviklingslande. En strategi for at løse dette problem indebærer befrugtning af afgrøder med
Håndtering af jern- og zinkmangel med bedre brødKredit:CC0 Public Domain Sundhedsmæssige virkninger af zink- og jernmangel kan være ødelæggende, især i udviklingslande. En strategi for at løse dette problem indebærer befrugtning af afgrøder med
- Hvorfor bliver bjerge mindre?
- Hvad er to store begivenheder, der skete i den kvartære periode?
- Hvad er forskellen mellem vækst og udvikling i en multicellulær organisme?
- Leder svovl elektricitet, når du er i vandig opløsning?
- Hvordan er det umuligt for et objekt i bevægelse på et givet tidspunkt?
- Et nyt magnetisk materiale og en optagelsesproces for at øge datakapaciteten markant


