Molaritet vs. normalitet:Hvad er mere koncentreret for H2SO4?
Forstå molaritet og normalitet
* Molaritet (M): Repræsenterer antallet af mol opløst stof pr. liter opløsning.
* Normalitet (N): Repræsenterer antallet af ækvivalenter af opløst stof pr. liter opløsning.
Nøgleforskel: Normalitet tager højde for antallet af *reaktive enheder* (f.eks. H+ ioner), et molekyle bidrager til en reaktion.
H2SO4 (Svovlsyre) Eksempel
* Molaritet: En 1 M H2SO4-opløsning indeholder 1 mol H2SO4 pr. liter opløsning.
* Normalitet: En 1 N H2SO4-opløsning indeholder 2 ækvivalenter H+-ioner pr. liter opløsning (da H2SO4 har 2 sure hydrogenatomer).
Konklusion
Da en 1 N H2SO4-opløsning indeholder 2 ækvivalenter H+-ioner pr. liter, mens en 1 M H2SO4-opløsning indeholder 1 mol H2SO4 pr. liter, er 1 N H2SO4-opløsningen mere koncentreret med hensyn til reaktive enheder (H+-ioner).
 Varme artikler
Varme artikler
-
 Softwareprogrammet Allchemy identificerer præbiotisk syntese af biokemiske forbindelser fra urpræk…Et team af forskere, der arbejder i Institut for Organisk Kemis laboratorium på det polske videnskabsakademi, har udviklet et softwareprodukt til at hjælpe med at opdage de kemiske processer, der ført
Softwareprogrammet Allchemy identificerer præbiotisk syntese af biokemiske forbindelser fra urpræk…Et team af forskere, der arbejder i Institut for Organisk Kemis laboratorium på det polske videnskabsakademi, har udviklet et softwareprodukt til at hjælpe med at opdage de kemiske processer, der ført -
 Videnskaben bag vaskemidler:hvordan de reducerer vandoverfladespændingenAf Athena Hessong Opdateret 24. marts 2022 Kwangmoozaa/iStock/GettyImages Detergentmolekyler har en meget smart egenskab, hvor den ene ende er hydrofil eller vandelskende, og den anden er hydrofob
Videnskaben bag vaskemidler:hvordan de reducerer vandoverfladespændingenAf Athena Hessong Opdateret 24. marts 2022 Kwangmoozaa/iStock/GettyImages Detergentmolekyler har en meget smart egenskab, hvor den ene ende er hydrofil eller vandelskende, og den anden er hydrofob -
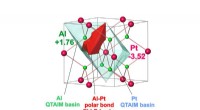 En elektrokatalysator til iltudviklingsreaktion ved vandspaltningAtomic QTAIM-bassiner af platin og aluminium (gennemsigtig) og Al-Pt-bindingsbassin (rød) i Al2Pt-forbindelsen, afslører den udtalte ladningsoverførsel fra Al- til Pt-atomer og polær karakter af Al-Pt
En elektrokatalysator til iltudviklingsreaktion ved vandspaltningAtomic QTAIM-bassiner af platin og aluminium (gennemsigtig) og Al-Pt-bindingsbassin (rød) i Al2Pt-forbindelsen, afslører den udtalte ladningsoverførsel fra Al- til Pt-atomer og polær karakter af Al-Pt -
 En fantastisk molekylær maskineDe adaptive iridocytter i huden på den californiske markedsblæksprutte er i stand til at indstille farven gennem det meste af spektret. Kredit:University of California - Santa Barbara blæksprutter
En fantastisk molekylær maskineDe adaptive iridocytter i huden på den californiske markedsblæksprutte er i stand til at indstille farven gennem det meste af spektret. Kredit:University of California - Santa Barbara blæksprutter
- Når to atomer kombineres ved at overføre elektroner, hvilken slags binding?
- Hvor skal jeg sidde for at få den bedste tur i en rutsjebane?
- Hvilken organelle forekommer cellulær respiration indeni?
- Mens Phoenix syder, by-ø-fænomen sammensætter varme (Opdatering)
- Hvordan laves frekvensen?
- Hvordan GEs nye Boston-hjem gik fra koldt til varmt (Opdatering)


