Hvorfor kaliumpermanganat ikke er tilberedt med HCl:En kemisk forklaring
Reaktion med HCl:
* Oxidationsreduktion: I denne reaktion virker permanganationen som et stærkt oxidationsmiddel, mens HCl virker som et reduktionsmiddel.
* Danning af klorgas: Permanganationen oxiderer chloridioner (Cl - ) fra HCl til dannelse af klorgas (Cl2 ).
* Mangan(II)-ioner: Permanganationen reduceres til mangan(II)-ioner (Mn 2+ ).
Den overordnede reaktion:
2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 5Cl2 + 8H2 O
Hvorfor er dette et problem for KMnO4 forberedelse:
* Ønsket produkt: Målet med at forberede KMnO4 er at opnå permanganation (MnO4 - ) i en stabil form.
* Reaktionsprodukter: Reaktionen med HCl genererer chlorgas og mangan(II)-ioner, som begge ikke er det ønskede produkt.
* Ineffektivitet: Reaktionen er spild, da den forbruger permanganationen uden at danne det ønskede produkt.
Alternative metoder:
I stedet for HCl, KMnO4 er typisk udarbejdet af:
* Elektrolyse: En elektrolytisk proces bruges til at oxidere mangan(II)-salte til permanganationer.
* Reaktion med kaliumhydroxid: Mangandioxid (MnO2 ) reageres med kaliumhydroxid (KOH) i nærværelse af et oxidationsmiddel som luft eller kaliumchlorat (KClO3 ).
Opsummering: Reaktionen mellem KMnO4 og HCl producerer uønskede biprodukter, hvilket gør det til en uegnet metode til fremstilling af kaliumpermanganat.
Sidste artikelBryde kovalente bindinger:Metoder og mekanismer
Næste artikelForståelse af kemiske underskrifter:Betydning og eksempler
 Varme artikler
Varme artikler
-
 Ny indsigt i fermenteringsenzymer vil sænke den kemiske industris CO2-fodaftrykForskere fra University of Tsukuba har opnået indsigt på atomniveau i strukturen af phosphoketolase-enzymet, hvilket vil hjælpe forskere med at optimere dette enzym til kemisk råstofsyntese. Kredit:
Ny indsigt i fermenteringsenzymer vil sænke den kemiske industris CO2-fodaftrykForskere fra University of Tsukuba har opnået indsigt på atomniveau i strukturen af phosphoketolase-enzymet, hvilket vil hjælpe forskere med at optimere dette enzym til kemisk råstofsyntese. Kredit: -
 Indvirkning af enzymkoncentration på reaktionshastigheder:Forståelse af forholdetJVisentin/iStock/GettyImages Enzymer er de usete motorer, der driver livets kemi. Uden dem ville vitale reaktioner forekomme for langsomt til at opretholde biologiske systemer. Men når enzymniveauet
Indvirkning af enzymkoncentration på reaktionshastigheder:Forståelse af forholdetJVisentin/iStock/GettyImages Enzymer er de usete motorer, der driver livets kemi. Uden dem ville vitale reaktioner forekomme for langsomt til at opretholde biologiske systemer. Men når enzymniveauet -
 Forskere udvikler unikke materialer til at reparere beskadigede organer og vævForskere skabte biokompatible og bioresorberbare polymermaterialer. Kredit:Peter den Store St. Petersborg Polytekniske Universitet Vævsteknologi er fremtiden for medicin. Polymer Materials for Tis
Forskere udvikler unikke materialer til at reparere beskadigede organer og vævForskere skabte biokompatible og bioresorberbare polymermaterialer. Kredit:Peter den Store St. Petersborg Polytekniske Universitet Vævsteknologi er fremtiden for medicin. Polymer Materials for Tis -
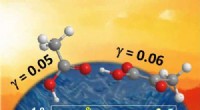 Carboxylsyrer opfører sig som supersyrer på overfladen af vandCarboxylsyrer opfører sig som supersyrer på luftsiden af vandoverfladen. Kredit:M. Guzman Atmosfæriske partikler med højt vandindhold også kendt som aerosoldråber findes i vid udstrækning på Jor
Carboxylsyrer opfører sig som supersyrer på overfladen af vandCarboxylsyrer opfører sig som supersyrer på luftsiden af vandoverfladen. Kredit:M. Guzman Atmosfæriske partikler med højt vandindhold også kendt som aerosoldråber findes i vid udstrækning på Jor
- Hvad er navnene på forskellige tåge?
- Hvilken aktivitet, der forekommer på solen, forårsager en aurora?
- Hvad er vigtigheden af ligevægt i undersøgelseskemiske reaktioner?
- Hvilke 2 biologiske variabler påvirker, hvor godt et enzym fungerer i kroppen?
- Hvorfor er hydrolorsyre opløst og vandopløsningsmiddel?
- Hvordan begyndte evolutionen?


