Bryde kovalente bindinger:Metoder og mekanismer
1. Energiinput:
* Varme: Forøgelse af temperaturen giver molekyler mere kinetisk energi, hvilket får dem til at vibrere kraftigere. Dette kan svække og til sidst bryde kovalente bindinger. Dette er grundlaget for mange kemiske reaktioner.
* Stråling: Elektromagnetisk stråling, såsom ultraviolet lys, kan også give energi til molekyler, hvilket fører til bindingsbrud. Sådan nedbryder UV-lys ozon i atmosfæren.
* Mekanisk kraft: Anvendelse af betydelig mekanisk kraft, såsom slibning eller knusning, kan også forstyrre kovalente bindinger. Dette er princippet bag mange kemiske reaktioner udført i kuglemøller.
2. Kemisk reaktivitet:
* Reaktion med andre molekyler: Introduktion af reaktive molekyler, der kan angribe og bryde de kovalente bindinger i de oprindelige molekyler. For eksempel kan en stærk syre protonere et molekyle, hvilket gør det mere modtageligt for at bryde dets bindinger.
* Introduktion af katalysatorer: Katalysatorer sænker den aktiveringsenergi, der kræves for at reaktioner kan forekomme, og accelererer således bindingsbrud. For eksempel er enzymer biologiske katalysatorer, der fremskynder reaktioner i levende organismer.
* Redox-reaktioner: Elektronoverførselsreaktioner, såsom oxidation eller reduktion, kan også bryde kovalente bindinger. For eksempel involverer forbrænding oxidation af et brændstofmolekyle med oxygen, hvilket resulterer i brydning af dets bindinger.
3. Fysiske processer:
* Opløsningsmiddeleffekter: Polære opløsningsmidler kan svække kovalente bindinger i polære molekyler ved at interagere med elektrondensitetsfordelingen. Dette skyldes, at polære molekyler er mere stabile, når de opløses i polære opløsningsmidler, som kan forstyrre de kovalente bindinger.
* Tryk: Stigende tryk kan også påvirke kovalent bindingsstyrke, men dette er mindre almindeligt end de andre metoder.
Det er vigtigt at bemærke, at:
* Klæbningsstyrken varierer meget: Forskellige kovalente bindinger har forskellige styrker. Nogle bindinger er meget stærke og kræver meget energi at bryde, mens andre er relativt svage og nemmere kan brydes.
* Specificitet er nøglen: Den metode du vælger til at destabilisere en kovalent binding vil afhænge af de specifikke molekyler og det ønskede resultat.
Samlet set kan forståelsen af de faktorer, der påvirker stabiliteten af kovalente bindinger, være afgørende for at designe og kontrollere kemiske reaktioner.
 Varme artikler
Varme artikler
-
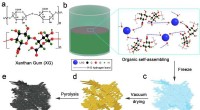 Forskere foreslår nye højtydende dual-ion-batterier med 3-D porøs strukturDannelsen af LTO@3DC -kompositmaterialet. Kredit:SIAT Dual-ion-batterier (DIBer) bestående af en grafitanode og katode har tiltrukket sig større opmærksomhed på grund af deres fordele ved miljøv
Forskere foreslår nye højtydende dual-ion-batterier med 3-D porøs strukturDannelsen af LTO@3DC -kompositmaterialet. Kredit:SIAT Dual-ion-batterier (DIBer) bestående af en grafitanode og katode har tiltrukket sig større opmærksomhed på grund af deres fordele ved miljøv -
 Konvektion vs. Advektion:Forståelse af de forskellige roller af varmeoverførsel i væskerAf Lee Johnson | Opdateret 30. august 2022 Hvad er konvektion? Konvektion er en flertrinsproces, der producerer cyklisk væskebevægelse, når en væske opvarmes. Et klassisk eksempel er vand i en gryde:
Konvektion vs. Advektion:Forståelse af de forskellige roller af varmeoverførsel i væskerAf Lee Johnson | Opdateret 30. august 2022 Hvad er konvektion? Konvektion er en flertrinsproces, der producerer cyklisk væskebevægelse, når en væske opvarmes. Et klassisk eksempel er vand i en gryde: -
 En ny måde at se, om der er genbrugsmateriale i den plastikflaske eller -poseTilføjelse af et fluorescerende mærke til genbrugsplast kan hjælpe med at spore deres mængde i nye engangsprodukter. Kredit:Tilpasset fra ACS Sustainable Chemistry &Engineering 2022 For at tilskynd
En ny måde at se, om der er genbrugsmateriale i den plastikflaske eller -poseTilføjelse af et fluorescerende mærke til genbrugsplast kan hjælpe med at spore deres mængde i nye engangsprodukter. Kredit:Tilpasset fra ACS Sustainable Chemistry &Engineering 2022 For at tilskynd -
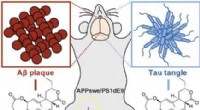 Rodbakterie til at bekæmpe Alzheimers:Rhizolutin adskiller beta- og tau-aggregaterKredit: Angewandte Chemie International Edition En bakterie fundet i jorden tæt på rødderne af ginsengplanter kunne give en ny tilgang til behandling af Alzheimers. Rhizolutin, en ny klasse af fo
Rodbakterie til at bekæmpe Alzheimers:Rhizolutin adskiller beta- og tau-aggregaterKredit: Angewandte Chemie International Edition En bakterie fundet i jorden tæt på rødderne af ginsengplanter kunne give en ny tilgang til behandling af Alzheimers. Rhizolutin, en ny klasse af fo
- Hvilket økosystem har frugtbar jord dækket med højt græs?
- Hvad er sandt med energi?
- Hvad er til stede i solen?
- Hvad er den krævede kraft for at give en masse på 10 kg en acceleration 5 ms²?
- Hvilke effekter får en asteroide, når den rammer jorden?
- Er der liv på Mars? Der skal bedre værktøjer til for at få svaret


