Beregning af pOH af ammoniak:En trin-for-trin guide
* Ammoniak er en svag base: Det ioniserer ikke fuldt ud i vand, hvilket betyder, at det ikke fuldstændigt donerer alle sine hydroxidioner (OH⁻).
* pOH afhænger af [OH⁻]: pOH af en opløsning beregnes ved hjælp af følgende formel:
pOH =-log[OH⁻]
For at finde ammoniakens pOH skal du bruge:
1. Koncentrationen af ammoniak: Dette udtrykkes normalt i molaritet (M).
2. Kb-værdien for ammoniak: Dette er basisioniseringskonstanten, som fortæller dig, i hvilket omfang ammoniak ioniseres i vand.
Sådan beregnes pOH:
1. Opret en ICE-tabel: Dette vil hjælpe dig med at spore ændringerne i koncentrationen, når ammoniak ioniserer.
```
NH3(aq) + H2O(l) ⇌ NH4+(aq) + OH⁻(aq)
Initial:[NH₃] 0 0
Ændre:-x +x +x
Ligevægt:[NH3]-x x x
```
2. Skriv Kb-udtrykket:
Kb =([NH₄⁺][OH⁻]) / [NH₃]
3. Substituer ligevægtskoncentrationerne fra ICE-tabellen og løs for x:
Kb =(x * x) / ([NH3] - x)
4. Løs for [OH⁻]:
[OH⁻] =x
5. Beregn pOH:
pOH =-log[OH⁻]
Eksempel:
Lad os sige, at du har en 0,1 M opløsning af ammoniak, og Kb for ammoniak er 1,8 x 10⁻⁵. Du ville følge trinene ovenfor for at beregne pOH.
Husk: pOH er et mål for hydroxidionkoncentration, og det er omvendt relateret til pH. Jo højere pOH, jo lavere er hydroxidkoncentrationen, og jo mere sur er opløsningen.
 Varme artikler
Varme artikler
-
 Knækker mysteriet om naturens hårdeste materialeMeget deformeret og genvundet perlemor. a Skematisk af den indvendige skaloverflade af toskallede bløddyr P. nobilis, med det undersøgte område markeret med en lilla firkant. b HAADF STEM oversigtsbil
Knækker mysteriet om naturens hårdeste materialeMeget deformeret og genvundet perlemor. a Skematisk af den indvendige skaloverflade af toskallede bløddyr P. nobilis, med det undersøgte område markeret med en lilla firkant. b HAADF STEM oversigtsbil -
 Næste generation af bærbare enheder forbliver ladet længere og sporer bevægelser bedreKredit:Negar Golestani Hvad hvis dit bælte gjorde mere end at holde bukserne op? Hvad hvis den også lyttede til din FitBit, smarte briller, og smarte smykker for bedre at genkende, hvilke aktivite
Næste generation af bærbare enheder forbliver ladet længere og sporer bevægelser bedreKredit:Negar Golestani Hvad hvis dit bælte gjorde mere end at holde bukserne op? Hvad hvis den også lyttede til din FitBit, smarte briller, og smarte smykker for bedre at genkende, hvilke aktivite -
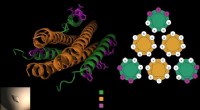 Forskere udvikler en bedre måde at blokere vira, der forårsager luftvejsinfektioner i barndommenDet antivirale peptid består af tre proptrækkere (i grønt), som låser sig omkring virussens fusionsprotein (i orange) for at forhindre virussen i at trænge ind i cellerne. Gellman-laboratoriet tilføje
Forskere udvikler en bedre måde at blokere vira, der forårsager luftvejsinfektioner i barndommenDet antivirale peptid består af tre proptrækkere (i grønt), som låser sig omkring virussens fusionsprotein (i orange) for at forhindre virussen i at trænge ind i cellerne. Gellman-laboratoriet tilføje -
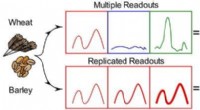 Et skridt i retning af følsom og hurtig glutenopdagelseKredit:American Chemical Society For mennesker med cøliaki og glutenfølsomhed, antallet af madmuligheder i butikkerne vokser. Men de nuværende test for gluten finder ikke alt stoffet i fødevarer,
Et skridt i retning af følsom og hurtig glutenopdagelseKredit:American Chemical Society For mennesker med cøliaki og glutenfølsomhed, antallet af madmuligheder i butikkerne vokser. Men de nuværende test for gluten finder ikke alt stoffet i fødevarer,
- Ulemperne ved bioteknologi
- Kan en enkelt magma producere flere forskellige stødende klipper med mineralkompositioner?
- Hvilke geologiske træk skabes af levende organismer?
- Hvad er retningen for acceleration på grund af tyngdekraften i opadgående bevægelse og nedadgåen…
- Hvilken videnskabsmand bestemte, at alle planter er lavet af celler?
- En mulig forklaring på et sæt observationer eller svar på videnskabeligt spørgsmål er en?


