Beregning af pH af en 10⁻⁵ M KOH-opløsning:en trin-for-trin guide
1. Forstå KOH
* KOH er kaliumhydroxid, en stærk base. Det betyder, at den dissocierer fuldstændigt i vand.
* Dissociationsreaktionen er:KOH (aq) → K⁺ (aq) + OH⁻ (aq)
2. Find hydroxidionkoncentrationen ([OH⁻])
* Da KOH er en stærk base, er koncentrationen af hydroxidioner ([OH⁻]) lig med startkoncentrationen af KOH:[OH⁻] =10⁻⁵ M
3. Beregning af pOH
* pOH er et mål for hydroxidionkoncentration:
pOH =-log[OH⁻]
pOH =-log(10-5) =5
4. Beregning af pH
* Forholdet mellem pH og pOH er:pH + pOH =14
* Derfor:pH =14 - pOH =14 - 5 =9
Svar: pH-værdien af en 10-5 M KOH-opløsning er 9 .
Sidste artikelBeregning af pH og pOH af en stærk baseopløsning
Næste artikelBeregn pOH af en HCl-opløsning:Trin-for-trin guide
 Varme artikler
Varme artikler
-
 Forstå Inconel:Sammensætning, applikationer og højtemperaturydelseAf Lexa W. Lee Opdateret 24. marts 2022 Bet_Noire/iStock/GettyImages Inconel er handelsnavnet for en gruppe på mere end 20 metallegeringer fremstillet af Special Metals Corporation. Legeringerne e
Forstå Inconel:Sammensætning, applikationer og højtemperaturydelseAf Lexa W. Lee Opdateret 24. marts 2022 Bet_Noire/iStock/GettyImages Inconel er handelsnavnet for en gruppe på mere end 20 metallegeringer fremstillet af Special Metals Corporation. Legeringerne e -
 Ingeniører udvikler et programmerbart camouflerende materiale inspireret af blækspruttehudSepia apama (gigantisk australsk blæksprutte), der udtrykker sine papiller til camouflageformål. Kredit:Roger Hanlon Til blæksprutten og blæksprutten, Øjeblikkeligt at ændre deres hudfarve og møn
Ingeniører udvikler et programmerbart camouflerende materiale inspireret af blækspruttehudSepia apama (gigantisk australsk blæksprutte), der udtrykker sine papiller til camouflageformål. Kredit:Roger Hanlon Til blæksprutten og blæksprutten, Øjeblikkeligt at ændre deres hudfarve og møn -
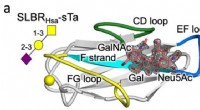 Udnyttelse af strukturen af bakterielle værtscellereceptorer til at påvise cancerKrystalstruktur af en streptococcus SLBR (Hsa) binding med høj affinitet til værtscellens glycanreceptor (sTa). Variation i sekvens og struktur af de mærkede SLBR-proteinsløjfer (CD, EF og FG) forudsi
Udnyttelse af strukturen af bakterielle værtscellereceptorer til at påvise cancerKrystalstruktur af en streptococcus SLBR (Hsa) binding med høj affinitet til værtscellens glycanreceptor (sTa). Variation i sekvens og struktur af de mærkede SLBR-proteinsløjfer (CD, EF og FG) forudsi -
 Forbindelser i en asiatisk fermenteret fiskepasta kan reducere højt kolesteroltalFermentering af karpefisk fører til frigivelse af forbindelser, der kan spille en rolle i at reducere kolesterolniveauet. Kredit:W.A. Djatmiko/C-C Wikimedia Forbindelser i en fermenteret fiskepast
Forbindelser i en asiatisk fermenteret fiskepasta kan reducere højt kolesteroltalFermentering af karpefisk fører til frigivelse af forbindelser, der kan spille en rolle i at reducere kolesterolniveauet. Kredit:W.A. Djatmiko/C-C Wikimedia Forbindelser i en fermenteret fiskepast
- 3D hierarkisk porøs nanostruktureret katalysator hjælper effektivt med at reducere kuldioxid
- Hvordan at lære mere om masseindlejring kan hjælpe med at bevare havskildpadder
- Jernkloridflammetest:Farve og hvorfor det er svært at observere
- Hvilken enhed bruges til opbevaring af den elektriske ladning?
- Rapportkort viser fortsat stigning i havniveauet ved øst- og golfkysten
- Hvad er de dele af planten, hvor kvindelige og mandlige gameter placeret?


