Krystal og molekylær strukturs indvirkning på ioniske og kovalente forbindelsers egenskaber
1. Smeltepunkt og kogepunkt:
* Ioniske forbindelser: Ioniske forbindelser har stærke elektrostatiske tiltrækninger mellem modsat ladede ioner. Disse kræfter er meget stærke og kræver meget energi at overvinde. Som et resultat har ioniske forbindelser høje smelte- og kogepunkter. Arrangementet af ioner i krystalgitteret påvirker også disse egenskaber. For eksempel fører et meget symmetrisk gitter som en ansigtscentreret kubisk (FCC) struktur generelt til højere smeltepunkter end et mindre symmetrisk gitter.
* Kovalente forbindelser: Kovalente forbindelser involverer deling af elektroner mellem atomer. Styrken af de intermolekylære kræfter (kræfter mellem molekyler) bestemmer deres smelte- og kogepunkter.
* Stærkere intermolekylære kræfter: Disse kræfter er til stede i kovalente forbindelser som hydrogenbundet vand, hvilket resulterer i højere smelte- og kogepunkter.
* Svagere intermolekylære kræfter: Kovalente forbindelser med svagere kræfter som London dispersionskræfter har lavere smelte- og kogepunkter. For eksempel har metan (CH4) et meget lavt kogepunkt på grund af svage intermolekylære kræfter.
2. Opløselighed:
* Ioniske forbindelser: Ioniske forbindelser har tendens til at være opløselige i polære opløsningsmidler som vand. Dette skyldes, at vandmolekyler har en delvis positiv ladning på brintatomerne og en delvis negativ ladning på iltatomet, hvilket giver dem mulighed for at interagere med ionerne og trække dem fra hinanden. Imidlertid er ioniske forbindelser generelt uopløselige i ikke-polære opløsningsmidler (som olie), fordi de ikke-polære opløsningsmiddelmolekyler ikke effektivt kan omgive de ladede ioner.
* Kovalente forbindelser: Kovalente forbindelser opløses generelt i opløsningsmidler, der har lignende intermolekylære kræfter.
* Polære kovalente forbindelser: Polære kovalente forbindelser som sukker (glukose) er opløselige i polære opløsningsmidler som vand. Dette skyldes, at både opløsningsmidlet og det opløste stof har lignende intermolekylære kræfter.
* Ikke-polære kovalente forbindelser: Ikke-polære kovalente forbindelser som olie er opløselige i ikke-polære opløsningsmidler som benzin. Dette skyldes, at de svage intermolekylære kræfter (London dispersionskræfter) i opløsningsmidlet kan overvinde de svage intermolekylære kræfter i det opløste stof.
Opsummering: Strukturen af en forbindelse spiller en afgørende rolle i at bestemme dens egenskaber. For ionforbindelser fører de stærke elektrostatiske kræfter på grund af krystalgitteret til høje smelte-/kogepunkter og opløselighed i polære opløsningsmidler. For kovalente forbindelser styrer styrken af intermolekylære kræfter mellem molekyler deres egenskaber, hvilket påvirker deres smelte-/kogepunkter og opløselighed i opløsningsmidler med lignende intermolekylære kræfter.
Sidste artikelFosforoxidationstilstand i PO33- Forklaret
Næste artikelEffektive metoder til adskillelse af forskellige faste stoffer
 Varme artikler
Varme artikler
-
 Hvordan formen påvirker en chokoladebars krystallinske strukturChokoladeforme påvirker chokoladens krystallinske struktur. Kredit:Popovphoto/Shutterstock.com Når du nyder en chokoladebar, de fleste mennesker tænker ikke over, hvordan molekylerne i det er orga
Hvordan formen påvirker en chokoladebars krystallinske strukturChokoladeforme påvirker chokoladens krystallinske struktur. Kredit:Popovphoto/Shutterstock.com Når du nyder en chokoladebar, de fleste mennesker tænker ikke over, hvordan molekylerne i det er orga -
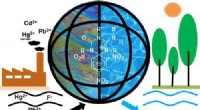 Let syntetiseret forbindelse fundet at være nyttig til at fjerne fluorid og metalioner fra drikkeva…Kredit:ACS (Phys.org) – Et par forskere ved Indian Institute of Science Education and Research Kolkata har fundet ud af, at en let syntetiseret forbindelse kan bruges til at fjerne fluorid og meta
Let syntetiseret forbindelse fundet at være nyttig til at fjerne fluorid og metalioner fra drikkeva…Kredit:ACS (Phys.org) – Et par forskere ved Indian Institute of Science Education and Research Kolkata har fundet ud af, at en let syntetiseret forbindelse kan bruges til at fjerne fluorid og meta -
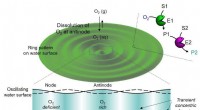 Spatiotemporal regulering af kemiske reaktioner ved kun at bruge hørbar lydFigur 1. Hørbar lydinduceret generering af transiente domæner og spatiotemporalt kontrollerede kaskadereaktionsnetværk. Kredit:Institut for Grundvidenskab Spatiotemporal regulering af flertrins enz
Spatiotemporal regulering af kemiske reaktioner ved kun at bruge hørbar lydFigur 1. Hørbar lydinduceret generering af transiente domæner og spatiotemporalt kontrollerede kaskadereaktionsnetværk. Kredit:Institut for Grundvidenskab Spatiotemporal regulering af flertrins enz -
 Ny genetisk metode forbedrer enzymets effektivitetGregg Beckham (til venstre), Christopher Johnson, og Jeffery Linger er medforfattere af en ny forskerartikel, der beskriver, hvordan de forbedrede effektiviteten af et enzym ved nedbrydning af bioma
Ny genetisk metode forbedrer enzymets effektivitetGregg Beckham (til venstre), Christopher Johnson, og Jeffery Linger er medforfattere af en ny forskerartikel, der beskriver, hvordan de forbedrede effektiviteten af et enzym ved nedbrydning af bioma
- Hvad gør et objekt til en planet?
- Åh min søster vær opmuntret Herren vil styrke dit hjerte Stormskyer forgår solen kommer til at s…
- Hvad sker der med partiklernes hastighed, hvis størrelsespartiklen øges?
- I hvilken rækkefølge forekommer videnskaberne for reproduktion fortrinsvis i flowdiagramform, så …
- Hvad er den 4.-Closest Planet til Sun?
- Bare tilsæt (kappe)vand:Ny forskning knækker mysteriet om, hvordan de første kontinenter blev til…


