Forstå den svage surhed af hydrogenfluorid (HF)
* Stærk hydrogenbinding: Fluor er det mest elektronegative grundstof, hvilket fører til en meget polær H-F-binding. Denne stærke polaritet resulterer i omfattende hydrogenbinding mellem HF-molekyler i opløsning. Hydrogenbindingerne er så stærke, at de effektivt "holder fast på" protonen (H+) og forhindrer den i let at dissociere til opløsning.
* Lille størrelse af fluor: Fluors lille størrelse giver mulighed for en meget tæt interaktion mellem fluoratomet og brintprotonen. Denne stærke interaktion hæmmer yderligere dissociationen af protonen.
* Lav dissociationskonstant: Dissociationskonstanten (Ka) for HF er betydeligt lavere end for andre stærke syrer som HCl, HBr og HI. Denne lave Ka indikerer, at kun en lille del af HF-molekyler dissocierer i opløsning, hvilket yderligere understøtter dens klassificering som en svag syre.
I modsætning til andre halogenider (HCl, HBr, HI) reducerer den stærke hydrogenbinding og den lille størrelse af fluor signifikant HFs tendens til at frigive protoner, hvilket gør det til en svag syre.
 Varme artikler
Varme artikler
-
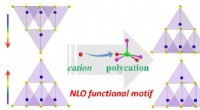 Bredspektrede NLO-materialer opnået ved polykation-substitution-induceret NLO-funktionel motivbesti…Skematisk illustration af rekonstruktion af NLO-funktionelt motiv på en parallel måde via polykation-substitution-induceret CS-til-NCS transformationsstrategi. Kredit:Prof. GUOs gruppe Ikke-lineær
Bredspektrede NLO-materialer opnået ved polykation-substitution-induceret NLO-funktionel motivbesti…Skematisk illustration af rekonstruktion af NLO-funktionelt motiv på en parallel måde via polykation-substitution-induceret CS-til-NCS transformationsstrategi. Kredit:Prof. GUOs gruppe Ikke-lineær -
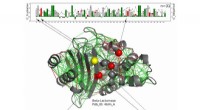 Arbejdsproteiner gør god brug af frustrationI denne strukturelle model for et beta-lactamase-protein, Katalytiske rester er vist som kugler med dem, der konsekvent er stærkt frustrerede langs hele beta-lactamase-familien vist med rødt, og dem,
Arbejdsproteiner gør god brug af frustrationI denne strukturelle model for et beta-lactamase-protein, Katalytiske rester er vist som kugler med dem, der konsekvent er stærkt frustrerede langs hele beta-lactamase-familien vist med rødt, og dem, -
 Filmfotosensibilisator:Meget effektiv singlet-iltgenerering(a) Fotos af kolonidannende enheder (CFU) for S. aureus inkuberet på LW-PBI-baserede film under bestråling med hvidt lys (90 mW/cm2, 10 min). (b) Absorbansplot registreret ved 291 nm af UA-opløsningen
Filmfotosensibilisator:Meget effektiv singlet-iltgenerering(a) Fotos af kolonidannende enheder (CFU) for S. aureus inkuberet på LW-PBI-baserede film under bestråling med hvidt lys (90 mW/cm2, 10 min). (b) Absorbansplot registreret ved 291 nm af UA-opløsningen -
 Næste generations 3D-trykte katalysatorer til at drive hypersonisk flyvningUdviklet som en del af NASAs Hyper-X-program, X-43A hypersonisk forskningskøretøj lavede luftfartshistorie i 2004, når hastigheder over Mach 9,6 eller over 10, 000 km/t. Kredit:NASA Ultraeffektive
Næste generations 3D-trykte katalysatorer til at drive hypersonisk flyvningUdviklet som en del af NASAs Hyper-X-program, X-43A hypersonisk forskningskøretøj lavede luftfartshistorie i 2004, når hastigheder over Mach 9,6 eller over 10, 000 km/t. Kredit:NASA Ultraeffektive
- Hvad er loven om bevaringsenergi et pinhjul?
- Undersøgelse viser, hvordan neuroner når deres endelige destinationer
- Er det sandt eller falsk destillation adskilt opløste stoffer gennem fysiske ændringer?
- Hvor mange sten er 150 lbs?
- Hvad er en enkelt sti for elektrisk strøm at strømme igennem?
- I henhold til celleteorien, hvor kommer alle celler fra?


