Afkodning af CoH2O6SO4:Hvorfor denne kemiske formel ikke eksisterer
Her er hvorfor:
* Kobolt (Co) er et overgangsmetal, og dets mest almindelige oxidationstilstande er +2 og +3.
* sulfat (SO4) har en ladning på -2.
* Vand (H2O) er et neutralt molekyle.
For at danne en neutral forbindelse skal ladningerne af kationerne og anionerne balancere. Lad os analysere mulighederne:
* Hvis Co har en +2-afgift: Sulfationen skal være til stede som SO4^2- for at balancere ladningen, men der er ingen måde at inkludere vandmolekyler for at få formlen til at fungere.
* Hvis Co har en +3-debitering: Sulfationen skal være til stede som SO4^2- for at balancere ladningen, men igen, der er ingen måde at inkludere vandmolekyler i formlen.
Mulige misforståelser:
* Skrivefejl: Det er muligt, at der er en tastefejl i formlen. Måske er den korrekte formel CoSO4.6H2O , som er en hydratiseret form af cobalt(II)sulfat kendt som Cobalt(II)sulfathexahydrat .
* Fejlfortolkning: Formlen kan være en gengivelse af en kompleks ion, men den er ikke klar uden mere kontekst.
For at få et gyldigt svar skal du sikre dig, at den kemiske formel er korrekt.
Sidste artikelAlkalimetaller:Forståelse af elektrontab og kationdannelse
Næste artikelForstå den svage surhed af hydrogenfluorid (HF)
 Varme artikler
Varme artikler
-
 Bæredygtigt vandbehandlingssystem inspireret af naturenStand Alone Sunflow System. Kredit:Monash University Studerende fra Monash Chemical Engineering har brugt den naturlige vandbehandlingscyklus fundet i naturen som inspiration til at udvikle en bær
Bæredygtigt vandbehandlingssystem inspireret af naturenStand Alone Sunflow System. Kredit:Monash University Studerende fra Monash Chemical Engineering har brugt den naturlige vandbehandlingscyklus fundet i naturen som inspiration til at udvikle en bær -
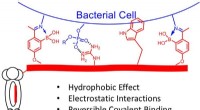 Team rapporterer teknologi, der muliggør præcisionsantibiotikaBoston College -forskere kemisk modificerede en fagvisning for at udvikle en ny tilgang til at finde specifikke bakteriestammer og målrette dem med antibiotika. Kredit: Journal of the American Chemica
Team rapporterer teknologi, der muliggør præcisionsantibiotikaBoston College -forskere kemisk modificerede en fagvisning for at udvikle en ny tilgang til at finde specifikke bakteriestammer og målrette dem med antibiotika. Kredit: Journal of the American Chemica -
 Sag løst:Forskere viser, hvordan det giftige nøddetræ danner strykninGiftnøddetræ Strychnos nux-vomica. Kredit:Danny Kessler, Max Planck Institute for Chemical Ecology Et forskerhold ved Max Planck Institute for Chemical Ecology i Jena afslørede den komplette biosyn
Sag løst:Forskere viser, hvordan det giftige nøddetræ danner strykninGiftnøddetræ Strychnos nux-vomica. Kredit:Danny Kessler, Max Planck Institute for Chemical Ecology Et forskerhold ved Max Planck Institute for Chemical Ecology i Jena afslørede den komplette biosyn -
 Kemiluminescensprober til hurtig og følsom påvisning af salmonella og listeriaKredit:CC0 Public Domain Salmonella og listeria er blandt de mest udbredte og dødeligste årsager til fødevarebårne infektioner. Deres hurtige og pålidelige registrering af fødevarer og industrielt
Kemiluminescensprober til hurtig og følsom påvisning af salmonella og listeriaKredit:CC0 Public Domain Salmonella og listeria er blandt de mest udbredte og dødeligste årsager til fødevarebårne infektioner. Deres hurtige og pålidelige registrering af fødevarer og industrielt
- Google-søgninger afslører, hvor folk er mest bekymrede over klimaændringer
- Comet 2019 LD2 (ATLAS) viste sig at være i aktiv overgang
- Stigende hav vil fortrænge millioner af mennesker – og Australien skal være klar
- Hvem erkendte, at stor energi frigives som et resultat af fusionshydrogenkerner til dannelse af deut…
- Sri Lanka forbyder plastik efter affaldskrise
- Hvad er en atmosfærefølende enhed?


