Jern(III)oxid (Fe₂O₃):Er det molekylært? Forståelse af ionisk binding
* Ionisk binding: Jern(III)oxid (Fe2O3) dannes gennem ionbinding. Jern (Fe) mister tre elektroner for at blive en positivt ladet ion (Fe³⁺), mens oxygen (O) får to elektroner til at blive en negativt ladet ion (O²⁻). Disse modsat ladede ioner tiltrækker hinanden elektrostatisk og danner en krystalgitterstruktur.
* Ingen diskrete molekyler: I ioniske forbindelser er der ingen særskilte, uafhængige molekyler. I stedet er ionerne arrangeret i et gentaget mønster gennem hele krystallen. Der er ikke et enkelt "molekyle" af Fe₂O₃.
Derimod:
* Molekylære forbindelser: Molekylære forbindelser dannes ved at dele elektroner mellem atomer (kovalent binding). Dette resulterer i distinkte, separate molekyler med et bestemt antal atomer. Eksempler inkluderer vand (H2O) og kuldioxid (CO2).
Derfor betragtes jern(III)oxid som en ionisk forbindelse, ikke en molekylær forbindelse.
 Varme artikler
Varme artikler
-
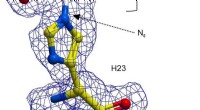 Kemikere viser, at det katalytiske udvalg af enzymer kan udvidesEn kugle-og-stik-repræsentation af H23 fra BH32 hæmmet med 2-bromacetophenon, farvet efter atomtype med H23 carbonatomer i gul og acetophenon carboner i hvid. Klar FEM elektrondensitet (blå, konturere
Kemikere viser, at det katalytiske udvalg af enzymer kan udvidesEn kugle-og-stik-repræsentation af H23 fra BH32 hæmmet med 2-bromacetophenon, farvet efter atomtype med H23 carbonatomer i gul og acetophenon carboner i hvid. Klar FEM elektrondensitet (blå, konturere -
 Tethered chem combos kunne revolutionere kunstig fotosynteseKlik på billedet for at downloade en version i høj opløsning.Brookhaven Lab kemiker Javier Concepcion og Lei Wang, en kandidatstuderende ved Stony Brook University, udtænkt et skema til samling af lys
Tethered chem combos kunne revolutionere kunstig fotosynteseKlik på billedet for at downloade en version i høj opløsning.Brookhaven Lab kemiker Javier Concepcion og Lei Wang, en kandidatstuderende ved Stony Brook University, udtænkt et skema til samling af lys -
 Producerer proteinbatterier for sikrere, miljøvenlig strømopbevaringKredit:CC0 Public Domain Proteiner er gode til at opbygge muskler, men deres byggeklodser kan også være nyttige til at bygge bæredygtige økologiske batterier, der en dag kan være en levedygtig ers
Producerer proteinbatterier for sikrere, miljøvenlig strømopbevaringKredit:CC0 Public Domain Proteiner er gode til at opbygge muskler, men deres byggeklodser kan også være nyttige til at bygge bæredygtige økologiske batterier, der en dag kan være en levedygtig ers -
 Sort silicium forhindrer øjenimplantat i at stivneKunstnerens skildring af et okulært implantat. Kredit:Lee, Jeong Oen, Vinayak Narasimhan, Juan Du, David W. Sretavan, og Hyuck Choo:Sort silicium som en biokompatibel antirefleksbelægning til medicins
Sort silicium forhindrer øjenimplantat i at stivneKunstnerens skildring af et okulært implantat. Kredit:Lee, Jeong Oen, Vinayak Narasimhan, Juan Du, David W. Sretavan, og Hyuck Choo:Sort silicium som en biokompatibel antirefleksbelægning til medicins
- Hvilken slags enkel maskine er der i en kuglepen?
- Vil du lære om dinosaurer? Saml noget Louisiana roadkill
- Elektronisk entropi forbedrer vandspaltning
- Forståelse af repræsentationen af encellede organismer
- Er klipper, der har fossiler i dem, normalt dannes fra dyr?
- Hvad er den kemiske formel for silikone og klor?


