Beregning af gasdensitet:Metoder og ideel gaslov
Forstå tæthed
Massefylde er defineret som masse pr. volumenenhed:
* Densitet (ρ) =Masse (m) / Volumen (V)
Metoder til at måle gasdensitet
1. Direkte metode (lov om ideel gas)
* Princip: Den ideelle gaslov giver et forhold mellem tryk (P), volumen (V), temperatur (T) og antallet af mol (n) af en gas:
* PV =nRT
* Hvor R er den ideelle gaskonstant.
* Procedure:
1. Mål trykket (P) af gassen ved hjælp af en trykmåler.
2. Mål volumen (V) af beholderen, der indeholder gassen.
3. Mål temperaturen (T) af gassen ved hjælp af et termometer.
4. Beregn antallet af mol (n) ved hjælp af den ideelle gaslovsligning.
5. Beregn massen (m) af gassen ved at bruge den molære masse (M) af gassen:
* m =n * M
6. Beregn tætheden (ρ) ved hjælp af formlen:ρ =m / V
2. Forskydningsmetode
* Princip: Denne metode er afhængig af gassens forskydning af et kendt volumen væske.
* Procedure:
1. Fyld en beholder med en kendt mængde væske (f.eks. vand).
2. Indfør gassen i beholderen, og fortræng noget af væsken.
3. Mål mængden af fortrængt væske.
4. Beregn massen af gassen ved hjælp af densiteten af den fortrængte væske og dens volumen.
5. Beregn tætheden (ρ) ved hjælp af formlen:ρ =m / V
Vigtige overvejelser:
* Temperatur og tryk: Gasdensiteten er meget følsom over for ændringer i temperatur og tryk. Sørg for, at du måler disse parametre nøjagtigt og opretholder konstante forhold under måleprocessen.
* Gasrenhed: Urenheder i gassen kan påvirke dens massefylde. Brug en ren gas eller tag hensyn til tilstedeværelsen af urenheder.
* Ideel gasadfærd: Den ideelle gaslov fungerer godt for mange gasser under normale forhold. Ved høje tryk eller lave temperaturer afviger reelle gasser dog fra den ideelle adfærd. I disse tilfælde kræves mere komplekse tilstandsligninger.
* Nøjagtighed: Nøjagtigheden af målingen afhænger af instrumenternes kvalitet og nøjagtigheden af målingerne.
Eksempel:
Lad os sige, at du har en beholder med et volumen på 1 liter fyldt med nitrogengas ved et tryk på 1 atmosfære og en temperatur på 25°C.
* Tryk (P): 1 atm
* Lydstyrke (V): 1 L
* Temperatur (T): 25°C + 273,15 =298,15 K
* Molar masse af nitrogen (M): 28,01 g/mol
* Ideel gaskonstant (R): 0,0821 L·atm/mol·K
Brug af den ideelle gaslov:
1. Beregn antallet af mol (n):
* n =(P * V) / (R * T) =(1 atm * 1 L) / (0,0821 L·atm/mol·K * 298,15 K) ≈ 0,0409 mol
2. Beregn massen (m):
* m =n * M =0,0409 mol * 28,01 g/mol ≈ 1,147 g
3. Beregn tætheden (ρ):
* ρ =m / V =1,147 g / 1 L =1,147 g/L
Derfor er tætheden af nitrogengas under disse forhold cirka 1,147 g/L.
 Varme artikler
Varme artikler
-
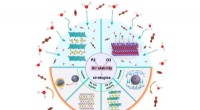 Luftstabilitet af natriumbaserede lagdelte oxidkatodematerialerAdskillige mekanismer og strategier blev vist i denne graf vedrørende luftfølsomheden af lagdelte natriumkatodematerialer. Kredit:Science China Press Natrium-ion-batterier anses for at være et af
Luftstabilitet af natriumbaserede lagdelte oxidkatodematerialerAdskillige mekanismer og strategier blev vist i denne graf vedrørende luftfølsomheden af lagdelte natriumkatodematerialer. Kredit:Science China Press Natrium-ion-batterier anses for at være et af -
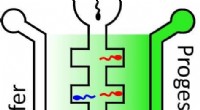 En ny måde at vurdere mandlig fertilitet påMere sædceller bevæger sig til højre side af en central kanal, som indeholder høje koncentrationer af progesteron (mørkegrøn), end til venstre side, som indeholder lavere koncentrationer (lysegrøn). K
En ny måde at vurdere mandlig fertilitet påMere sædceller bevæger sig til højre side af en central kanal, som indeholder høje koncentrationer af progesteron (mørkegrøn), end til venstre side, som indeholder lavere koncentrationer (lysegrøn). K -
 Denne hydrogeltablet kan rense en liter flodvand på en timeBrug af hydrogel-tabletten til at rense vand kræver ingen energitilførsel og skaber ikke skadelige biprodukter. Kredit:University of Texas i Austin. Så meget som en tredjedel af verdens befolkning
Denne hydrogeltablet kan rense en liter flodvand på en timeBrug af hydrogel-tabletten til at rense vand kræver ingen energitilførsel og skaber ikke skadelige biprodukter. Kredit:University of Texas i Austin. Så meget som en tredjedel af verdens befolkning -
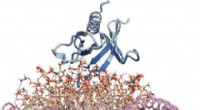 Indsigt på atomniveau opnået for et vigtigt lipidbindende protein impliceret i kræftNanodisk erstatning cellemembran:Protein er blåt, lipider er hvede, og de to spiralformede lipoproteiner, der holder lipid-nanoskiven sammen, er lyserøde. Kredit:Sanford Burnham Prebys Medical Discove
Indsigt på atomniveau opnået for et vigtigt lipidbindende protein impliceret i kræftNanodisk erstatning cellemembran:Protein er blåt, lipider er hvede, og de to spiralformede lipoproteiner, der holder lipid-nanoskiven sammen, er lyserøde. Kredit:Sanford Burnham Prebys Medical Discove
- Hvordan hjalp Griffith med at opbygge vores forståelse af genetisk?
- Hvem var den første sorte astronaunt, der gik i rummet?
- Sådan viser du undersøgelsesprocent
- Dette er hvorfor Fortnite er så Addictive
- Små fossiler afslører, hvordan krympning var afgørende for en vellykket evolution
- Hvilken energioverførsel finder sted, når dampen hvad der kommer ind i turbinhuset?


