Forståelse af hydrofile opløste stoffer:Egenskaber og eksempler
Her er en opdeling:
* Polaritet: Vand er et polært molekyle, hvilket betyder, at det har en positiv ende og en negativ ende. Dette gør det muligt at danne stærke bindinger med andre polære molekyler.
* Hydrofile opløste stoffer: Disse opløste stoffer er også polære og indeholder ladede grupper eller polære funktionelle grupper som hydroxyl (-OH), carboxyl (-COOH) eller amin (-NH2) grupper. Disse grupper kan danne hydrogenbindinger med vand, hvilket gør dem letopløselige.
Eksempler på hydrofile opløste stoffer omfatter:
* Sukker: Glucose, fructose, saccharose
* Salte: Natriumchlorid (NaCl)
* Syrer: Citronsyre, eddikesyre
* Alkoholer: Ethanol, methanol
* Aminosyrer: Byggestenene til proteiner
Derimod:
* Hydrofobe opløste stoffer er ikke-polære og opløses ikke let i vand. De tiltrækkes af andre ikke-polære molekyler og har tendens til at klumpe sig sammen i vand. Eksempler omfatter fedtstoffer, olier og voks.
Sidste artikelPolysaccharider:Forståelse af komplekse kulhydrater
Næste artikelBeregning af gasdensitet:Metoder og ideel gaslov
 Varme artikler
Varme artikler
-
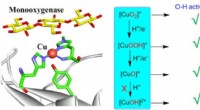 Teoretisk perspektiv på C-H/O-H-aktivering af Cu-O i biologiske og syntetiske systemerDioxygenaktivering med mononukleært kobber i biologiske og syntetiske systemer kan generere forskellige kobber-oxygen-mellemprodukter, herunder [CuO2 ]+ , [CuOOH]+ , [CuO]+ , [CuOH]2+ . Alle disse art
Teoretisk perspektiv på C-H/O-H-aktivering af Cu-O i biologiske og syntetiske systemerDioxygenaktivering med mononukleært kobber i biologiske og syntetiske systemer kan generere forskellige kobber-oxygen-mellemprodukter, herunder [CuO2 ]+ , [CuOOH]+ , [CuO]+ , [CuOH]2+ . Alle disse art -
 Hvad er en vandig opløsning? Et klart overblikSinhyu/iStock/GettyImages En vandig opløsning er en blanding, hvori vand tjener som opløsningsmiddel og opløser et eller flere opløste stoffer. Mens vand oftest forekommer som en væske ved stuetemper
Hvad er en vandig opløsning? Et klart overblikSinhyu/iStock/GettyImages En vandig opløsning er en blanding, hvori vand tjener som opløsningsmiddel og opløser et eller flere opløste stoffer. Mens vand oftest forekommer som en væske ved stuetemper -
 Forskere udvikler hurtig og enkel metode til påvisning af glyphosatProfessor Tilo Pompe (tv) og doktorgradsforsker David Rettke fra Institut for Biokemi er ved at udvikle en metode til hurtig påvisning af glyphosat. Kredit:Swen Reichhold, Leipzig Universitet Glyp
Forskere udvikler hurtig og enkel metode til påvisning af glyphosatProfessor Tilo Pompe (tv) og doktorgradsforsker David Rettke fra Institut for Biokemi er ved at udvikle en metode til hurtig påvisning af glyphosat. Kredit:Swen Reichhold, Leipzig Universitet Glyp -
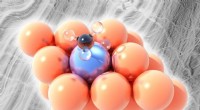 Omdannelse af gas til brændstoffer med bedre legeringerAfbildet, platin-kobber enkeltatom legeringen. Kobber (orange) er ude af stand til at bryde bindinger mellem kulstof (sort) og brint (klart) i metanderivater undtagen ved højere temperaturer, men et e
Omdannelse af gas til brændstoffer med bedre legeringerAfbildet, platin-kobber enkeltatom legeringen. Kobber (orange) er ude af stand til at bryde bindinger mellem kulstof (sort) og brint (klart) i metanderivater undtagen ved højere temperaturer, men et e
- Hvilke to levesteder er i neritisk zone?
- Genbrug og genbrug af slidte katoder til at lave nye lithium-ion-batterier
- Hvad kaldes overførslen af varme gennem elektromagnetisk aktivitet?
- Hvad er en blanding af mineraler mineraloider glas eller organisk stof?
- Hvad er valenscelle?
- Hvad er tætheden af dekan?


