Forklaret kogepunkt:Faktorer, der påvirker væske- til gasovergangen
* Kogepunktet afhænger af trykket: Jo lavere tryk, jo lavere kogepunkt. Derfor koger vand ved en lavere temperatur på en bjergtop end ved havoverfladen.
* Forskellige væsker har forskellige kogepunkter: Vand koger ved 100°C (212°F) ved standardatmosfærisk tryk, men ethanol koger ved 78,37°C (173°F).
For at bestemme kogepunktet for en bestemt væske skal du kende det tryk, som den opvarmes til.
Her er nogle yderligere punkter:
* Fordampning: Væsker kan blive til gas under deres kogepunkt gennem en proces kaldet fordampning. Dette sker, fordi nogle molekyler har nok energi til at undslippe væskeoverfladen.
* Damptryk: Selv ved temperaturer under kogepunktet har væsker et damptryk, som er det tryk, som gasmolekylerne udøver over væskeoverfladen.
Sig til, hvis du gerne vil vide mere om disse koncepter!
Sidste artikelKogepunkt:Forståelse af temperaturen ved faseændring
Næste artikelKogepunkt Forklaret:Forståelse af damptryk og eksternt tryk
 Varme artikler
Varme artikler
-
 En måde at øge strukturel stabilitet i anstrengte halogenidperovskitteren, Optiske billeder af de voksende epitaksiale α-FAPbI3 tynde film. Den høje gennemsigtighed af substraterne og de glatte overflader af de tynde film demonstrerer deres høje kvalitet. Målestænger, 4
En måde at øge strukturel stabilitet i anstrengte halogenidperovskitteren, Optiske billeder af de voksende epitaksiale α-FAPbI3 tynde film. Den høje gennemsigtighed af substraterne og de glatte overflader af de tynde film demonstrerer deres høje kvalitet. Målestænger, 4 -
 Forbedring af limningen af plast i højpræcisions mikrofluidchipsMikrofluidchips gør det muligt at analysere en dråbe blod næsten øjeblikkeligt og har potentialet til at revolutionere sundhedsvæsenet. Kredit:A*STAR Singapore Institute of Manufacturing Technology
Forbedring af limningen af plast i højpræcisions mikrofluidchipsMikrofluidchips gør det muligt at analysere en dråbe blod næsten øjeblikkeligt og har potentialet til at revolutionere sundhedsvæsenet. Kredit:A*STAR Singapore Institute of Manufacturing Technology -
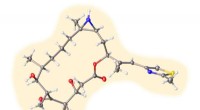 Lab skaber hårde, men øm, kræftkæmpereStruktur af en af analogerne til epothilon B, en ny forbindelse oprettet i Rice University lab af syntetisk organisk kemiker K.C. Nicolaou, der viser løfte som kræftkæmper. Kredit:Nicolaou Group/Ric
Lab skaber hårde, men øm, kræftkæmpereStruktur af en af analogerne til epothilon B, en ny forbindelse oprettet i Rice University lab af syntetisk organisk kemiker K.C. Nicolaou, der viser løfte som kræftkæmper. Kredit:Nicolaou Group/Ric -
 Formændrende element har nøglen til antibakteriel belægningAfbildet fra venstre til højre:University of Canterbury ph.d.-studerende Rukmini Gorthy og Johann Land og forskningsleder Maskin- og materialteknik Professor Susan Krumdieck er medforfattere på et pap
Formændrende element har nøglen til antibakteriel belægningAfbildet fra venstre til højre:University of Canterbury ph.d.-studerende Rukmini Gorthy og Johann Land og forskningsleder Maskin- og materialteknik Professor Susan Krumdieck er medforfattere på et pap
- Transform Boundaries:Hvordan de skulpturerer jordens overflade
- Hvad er din idé til at 3D-printe på månen – få det til at føles som hjemme?
- Hvad bruges enheden til at måle strålende energi?
- Hvad er procentdelen af masse af ilt i CaOH2 -formlen 74.1?
- Hvad er retningsacceleration?
- Hvilke beviser har du for, at ligevægten skiftede, når mættet kaliumnitratopløsning blev afkøle…


