Reaktivitetssammenligning:Gruppe 13 vs. Gruppe 1 Metaller - Kemiske principper
* Elektronkonfiguration: Gruppe 1 metaller har en valenselektron, som de let mister for at danne en +1 kation. Gruppe 13 metaller har tre valenselektroner. Mens de kan miste disse elektroner for at danne en +3 kation, kræver det mere energi at fjerne tre elektroner sammenlignet med en.
* Ioniseringsenergi: Ioniseringsenergi er den energi, der kræves for at fjerne en elektron fra et atom. Gruppe 13 metaller har højere ioniseringsenergier end gruppe 1 metaller, hvilket gør dem mindre tilbøjelige til at miste elektroner.
* Metallig karakter: Når du bevæger dig hen over en periode i det periodiske system, falder det metalliske karakter. Dette betyder, at gruppe 13-metaller er mindre metalliske og derfor mindre reaktive end gruppe 1-metaller.
Opsummering, reaktiviteten af metaller i det periodiske system falder, når du bevæger dig fra venstre mod højre over en periode (på grund af stigende ioniseringsenergi og faldende metallisk karakter).
 Varme artikler
Varme artikler
-
 Svampeforbindelser hæmmer en vigtig gruppe af proteinerSvampen, der producerer cercosporamid. Kredit:Jelmer Hoeksma, copyright Hubrecht Institute Forskere i Jeroen den Hertogs gruppe, i samarbejde med forskere i Leiden, har fundet ud af, at en forbind
Svampeforbindelser hæmmer en vigtig gruppe af proteinerSvampen, der producerer cercosporamid. Kredit:Jelmer Hoeksma, copyright Hubrecht Institute Forskere i Jeroen den Hertogs gruppe, i samarbejde med forskere i Leiden, har fundet ud af, at en forbind -
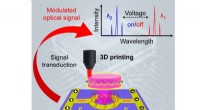 Ny rekord:3-D-printet optisk-elektronisk integrationSkematisk illustration af et integreret elektrisk styret mikrolasermodul til optoelektronisk hybridintegration. Kort, dette modul er designet til at være en termo-responsiv polymerresonator oven på et
Ny rekord:3-D-printet optisk-elektronisk integrationSkematisk illustration af et integreret elektrisk styret mikrolasermodul til optoelektronisk hybridintegration. Kort, dette modul er designet til at være en termo-responsiv polymerresonator oven på et -
 Nye topologiske materialer kan have flere elektriske egenskaberDen består af seks Dirac-kegler (placeret på den stiplede cirkel), der repræsenterer de krystallinske topologiske tilstande, der sameksisterer med 1D lineært spektrum (Xet i midten), der repræsenterer
Nye topologiske materialer kan have flere elektriske egenskaberDen består af seks Dirac-kegler (placeret på den stiplede cirkel), der repræsenterer de krystallinske topologiske tilstande, der sameksisterer med 1D lineært spektrum (Xet i midten), der repræsenterer -
 Video:Hvad er kemien bag ringorm?Vidste du, at ringorm faktisk ikke er en orm? Denne uge om reaktioner, find ud af hvad ringorm er; hvordan den skyldige lever af din hud, hår og negle; og hvordan man ikke bliver det næste måltid:
Video:Hvad er kemien bag ringorm?Vidste du, at ringorm faktisk ikke er en orm? Denne uge om reaktioner, find ud af hvad ringorm er; hvordan den skyldige lever af din hud, hår og negle; og hvordan man ikke bliver det næste måltid:
- Hvorfor videnskaben har brug for humaniora for at løse klimaændringer
- Amerikansk cybersikkerhedsfirma:Hackere stjal EU's diplomatiske kabler
- Hvor i Europa vil det næste skadedyrsangreb forekomme?
- Ståer Venuses solen op og sætter det samme som Jorden?
- Hvad er den kinetiske energi i en 1500 kg bil, der bevæger sig ved følgende hastigheder 29ms 18ms …
- Bioøkonomien:Leverer bæredygtig grøn vækst?


