Forståelse af kemisk reaktionshastighed:Faktorer og måling
Her er en oversigt over hovedpunkterne:
* Ændring i koncentration: Det kan være faldet i koncentrationen af en reaktant eller stigningen i koncentrationen af et produkt.
* Enhedstid: Det tidsinterval, hvor koncentrationsændringen måles, ofte sekunder, minutter eller timer.
Faktorer, der påvirker reaktionsfrekvensen:
Flere faktorer påvirker hastigheden af en kemisk reaktion, herunder:
* Temperatur: Højere temperaturer fører generelt til hurtigere reaktionshastigheder.
* Koncentration: Højere koncentrationer af reaktanter fører ofte til hurtigere hastigheder.
* Overfladeareal: Øget overfladeareal af reaktanter, som i pulvere eller findelte faste stoffer, kan øge reaktionshastigheden.
* Katalysator: En katalysator fremskynder en reaktion uden at blive forbrugt i processen.
* Reaktanternes art: Forskellige reaktanter reagerer med forskellige hastigheder.
Reaktionsenheder:
Enhederne for reaktionshastighed afhænger af rækkefølgen af reaktionen, men almindeligt anvendte enheder omfatter:
* M/s (mol i sekundet)
* mol/L·s (mol pr. liter pr. sekund)
Betydning af reaktionsfrekvens:
Forståelse af reaktionshastigheder er afgørende på forskellige områder:
* Kemi: At studere reaktionsmekanismer og kinetik.
* Kemiteknik: Design og optimering af kemiske processer.
* Biologi: Undersøgelse af enzymkinetik og metaboliske veje.
* Medicin: Forståelse af stofskifte og effektivitet.
Lad mig vide, hvis du vil have en mere detaljeret forklaring på nogle af disse aspekter eller ønsker at lære om specifikke typer kemiske reaktioner.
 Varme artikler
Varme artikler
-
 Grønt vandrensningssystem fungerer uden tungmetaller eller ætsende kemikalierDette billede viser en koncentrator, hvor prøver blev placeret. Kredit:Dan Wang Forskere ved Institute of Process Engineering (IPE) ved det kinesiske videnskabsakademi i Beijing og Yangzhou Univer
Grønt vandrensningssystem fungerer uden tungmetaller eller ætsende kemikalierDette billede viser en koncentrator, hvor prøver blev placeret. Kredit:Dan Wang Forskere ved Institute of Process Engineering (IPE) ved det kinesiske videnskabsakademi i Beijing og Yangzhou Univer -
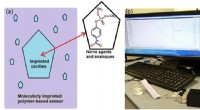 Hurtig påvisning af giftige forbindelserFigur viser (a) princippet for MIP-baserede sensorer, hvor unikke mønstre af målmolekylerne er præget på en polymerbaseret sensorfilm og (b) et eksperiment udføres ved hjælp af den MIP-baserede sensor
Hurtig påvisning af giftige forbindelserFigur viser (a) princippet for MIP-baserede sensorer, hvor unikke mønstre af målmolekylerne er præget på en polymerbaseret sensorfilm og (b) et eksperiment udføres ved hjælp af den MIP-baserede sensor -
 Et multidimensionelt billede af SARS-CoV-2En massespektrometeranordning (detaljer):Ved hjælp af massespektrometrisk analyse ved Max Planck Institute of Biochemistry, forskerne opdagede 1484 interaktioner mellem virale og humane cellulære prot
Et multidimensionelt billede af SARS-CoV-2En massespektrometeranordning (detaljer):Ved hjælp af massespektrometrisk analyse ved Max Planck Institute of Biochemistry, forskerne opdagede 1484 interaktioner mellem virale og humane cellulære prot -
 Hvordan fortynding af eddike sænker dens surhed:pH-effekten forklaretAf Claire Gillespie Opdateret 24. marts 2022 YelenaYemchuk/iStock/GettyImages Når en syre som eddike fortyndes med vand, falder koncentrationen af fritflydende hydrogenioner. Dette resulterer i en
Hvordan fortynding af eddike sænker dens surhed:pH-effekten forklaretAf Claire Gillespie Opdateret 24. marts 2022 YelenaYemchuk/iStock/GettyImages Når en syre som eddike fortyndes med vand, falder koncentrationen af fritflydende hydrogenioner. Dette resulterer i en
- Angiv hvilken mad der bruges til af kroppen?
- Ekspertvejledning til lokalisering af kobberaflejringer
- Forskere udvikler en ny ikke-målrettet screeningsmetode for fødevaresikkerhed fra dyr
- Hvad er en landform med relativ flad top?
- Ny forskning afslører, hvordan man kan afgifte snavs - zap det med lasere
- Nye historiske emissionstendenser estimeret med fællesskabets emissionsdatasystem


