Carbon Catenation:Forståelse af dannelsen af organiske forbindelser
Cateneringsegenskaber for kulstof:
Catenation er et elements evne til at danne lange kæder med sig selv. Kulstof udviser denne egenskab på en bemærkelsesværdig måde, hvilket fører til dannelsen af en bred vifte af organiske forbindelser. Her er en oversigt over dens kateneringsegenskaber:
Nøglefunktioner:
* Stærke kulstof-kulstofbindinger: Kulstof danner stærke kovalente bindinger med sig selv på grund af dets lille størrelse og fire valenselektroner. Dette fører til stabile kæder og ringe.
* Tetraedrisk geometri: Carbons fire valenselektroner tillader det at danne fire bindinger med andre atomer, hvilket resulterer i en tetraedrisk geometri. Dette giver fleksibilitet til bindingsarrangementer.
* Forskellige obligationstyper: Kulstof kan danne enkelt-, dobbelt- og tredobbeltbindinger med sig selv, hvilket øger mangfoldigheden af mulige strukturer.
* Danning af ringe: Kulstof danner let lukkede ringstrukturer, hvilket øger kompleksiteten af organiske molekyler.
Konsekvenser af katenering:
* Enormt antal organiske forbindelser: Kulstoffets unikke egenskaber muliggør dannelsen af millioner af forskellige organiske forbindelser med varierende strukturer og egenskaber.
* Livsgrundlag: Carbons kædeevne er afgørende for livet. Det danner rygraden i essentielle biomolekyler som kulhydrater, lipider, proteiner og nukleinsyrer.
* Industriel betydning: Carbons kædeegenskaber udnyttes i mange industrielle applikationer, herunder plastik, brændstoffer og lægemidler.
Faktorer, der påvirker katenering:
* Forbindelsesstyrke: Stærkere carbon-carbon-bindinger forbedrer kædedannelse.
* Forbindelseslængde: Kortere bindingslængder fremmer stabilitet og katenering.
* Elektronegativitet: Carbons moderate elektronegativitet gør det muligt for det at danne stabile bindinger med forskellige elementer.
Sammenligning med andre elementer:
Mens andre elementer kan udvise katenering, er kulstofs evne uovertruffen på grund af kombinationen af faktorer nævnt ovenfor. Silicium danner for eksempel kæder, men med væsentligt svagere bindinger, hvilket fører til mindre forskellige strukturer.
Opsummering:
Carbons kædeegenskaber med dets stærke bindinger, fleksible geometri og alsidighed i bindingstyper er ansvarlig for den enorme mangfoldighed og kompleksitet af organiske forbindelser, hvilket i sidste ende understøtter liv og adskillige industrielle anvendelser.
Sidste artikelKulsammensætning:Forstå dens kemiske kompleksitet
Næste artikelForstå løsningskoncentration:En omfattende vejledning
 Varme artikler
Varme artikler
-
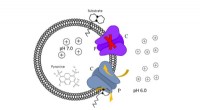 Arbejder på at opdage nye behandlinger mod tuberkuloseMmpL3 er det vigtigste mål for opdagelsen af nye anti-tuberkuloselægemidler. Zgurskaya og medforfattere isolerede dette mål fra bakterieceller og rekonstituerede det i kunstige membraner. Dette skab
Arbejder på at opdage nye behandlinger mod tuberkuloseMmpL3 er det vigtigste mål for opdagelsen af nye anti-tuberkuloselægemidler. Zgurskaya og medforfattere isolerede dette mål fra bakterieceller og rekonstituerede det i kunstige membraner. Dette skab -
 Selvsamlende peptider og kampen mod fedme og diabetesFibriller af peptidhormonet Oxyntomodulin, med diametre fra ~6 til 40 nm. Kredit:S. Kinna Et samarbejde mellem Afdelingens Nanoscience Center og MedImmune tager store skridt mod en sikrere og mere
Selvsamlende peptider og kampen mod fedme og diabetesFibriller af peptidhormonet Oxyntomodulin, med diametre fra ~6 til 40 nm. Kredit:S. Kinna Et samarbejde mellem Afdelingens Nanoscience Center og MedImmune tager store skridt mod en sikrere og mere -
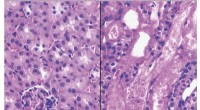 Anti-aldringsmolekylet NAD+ får et løft ved at blokere et enzymHistologisk snit af en normal nyre (venstre) versus en nyre efter akut nyreskade (højre). Kredit:J. Auwerx, EPFL Nikotinamid adenin dinukleotid (NAD+) er en vigtig spiller inden for ernæring i dag
Anti-aldringsmolekylet NAD+ får et løft ved at blokere et enzymHistologisk snit af en normal nyre (venstre) versus en nyre efter akut nyreskade (højre). Kredit:J. Auwerx, EPFL Nikotinamid adenin dinukleotid (NAD+) er en vigtig spiller inden for ernæring i dag -
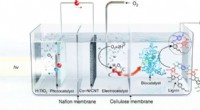 Nyt biokatalytisk system gør affaldsbiomasse til værdiskabende kemikalierSkematisk illustration af den tre-rums foto-elektro-biokemiske reaktor. Kredit:UNIST Et forskerhold, i fællesskab ledet af professor Ji Wook Jang, Professor Yong Hwan Kim, og professor Sang Hoon J
Nyt biokatalytisk system gør affaldsbiomasse til værdiskabende kemikalierSkematisk illustration af den tre-rums foto-elektro-biokemiske reaktor. Kredit:UNIST Et forskerhold, i fællesskab ledet af professor Ji Wook Jang, Professor Yong Hwan Kim, og professor Sang Hoon J
- Hvor mange argon atomer kan passe på overfladen af et kulstof nanorør?
- Forståelse af formelenhedsafgift:hvorfor den altid er nul
- Hvad betyder klassificering i en videnskabelig sigt?
- Hvad er en kaustisk base?
- Hvor er den arvelige information om en organisme?
- Udviklede det tokammersindede sig til at skabe moderne menneskelig bevidsthed?


