Forstå forholdet mellem pH og hydroniumionkoncentration
* pH-skala: pH-skalaen måler surhedsgraden eller alkaliniteten af en opløsning. Det går fra 0 til 14, med:
* 0 til 6,9: Sure opløsninger (højere H₃O⁺-koncentration)
* 7: Neutral opløsning (lig H₃O⁺ og OH⁻ koncentration)
* 7,1 til 14: Basiske eller alkaliske opløsninger (lavere H₃O⁺-koncentration)
* Forholdet: pH beregnes ved hjælp af følgende ligning:
pH =-log[H3O+]
hvor [H3O+] repræsenterer koncentrationen af hydroniumioner i mol pr. liter (M).
* Nøglepunkter:
* Når koncentrationen af hydroniumioner stiger , pH falder (mere syrlig).
* Når koncentrationen af hydroniumioner falder , pH stiger (mere basisk).
Eksempel:
* En opløsning med en hydroniumionkoncentration på 1 x 10⁻4 M har en pH på 4.
* En opløsning med en hydroniumionkoncentration på 1 x 10⁻¹⁰ M har en pH-værdi på 10.
Opsummering:
* Højere [H₃O⁺] =Lavere pH (surere)
* Lavere [H₃O⁺] =Højere pH (mere basisk)
 Varme artikler
Varme artikler
-
 En molekylær dans af fosfolipidsynteseCCT er et nøgleenzym, der opretholder en afbalanceret sammensætning af cellemembranfosfolipider. Billedet fremhæver dynamikken i en del af enzymet CCT, der er afgørende for regulering af dets funktion
En molekylær dans af fosfolipidsynteseCCT er et nøgleenzym, der opretholder en afbalanceret sammensætning af cellemembranfosfolipider. Billedet fremhæver dynamikken i en del af enzymet CCT, der er afgørende for regulering af dets funktion -
 Byg en klasseværelsesmodel af uranatomet – trin-for-trin-vejledningUran (symbol U) spiller en central rolle i både elproduktion og national sikkerhed. Dens evne til at gennemgå nuklear fission gør den til et nøgleelement i reaktorer og våben. Opbygning af en fysisk m
Byg en klasseværelsesmodel af uranatomet – trin-for-trin-vejledningUran (symbol U) spiller en central rolle i både elproduktion og national sikkerhed. Dens evne til at gennemgå nuklear fission gør den til et nøgleelement i reaktorer og våben. Opbygning af en fysisk m -
 Video:Hvorfor du ikke kan købe friske olivenKredit:The American Chemical Society Oliven vokser på træer. Så hvorfor har du aldrig set en frisk, træmodnet oliven i produktafdelingen i købmanden? Hvorfor svømmer de altid i saltlage? Åh, og
Video:Hvorfor du ikke kan købe friske olivenKredit:The American Chemical Society Oliven vokser på træer. Så hvorfor har du aldrig set en frisk, træmodnet oliven i produktafdelingen i købmanden? Hvorfor svømmer de altid i saltlage? Åh, og -
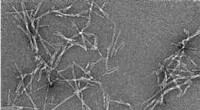 Forstå væksten af sygdomsfremkaldende proteinfibreTransmissionselektronmikrofotografi af fibriller fra proteinet alfa-synuclein, som er forbundet med Parkinsons sygdom. Kredit:University of Bath Amyloidfibriller er aflejringer af proteiner i krop
Forstå væksten af sygdomsfremkaldende proteinfibreTransmissionselektronmikrofotografi af fibriller fra proteinet alfa-synuclein, som er forbundet med Parkinsons sygdom. Kredit:University of Bath Amyloidfibriller er aflejringer af proteiner i krop
- Fordelene ved kondensator Start & Kondensator Kør Motorer
- Hvor findes DNA specifikt i vores celler?
- Kvantificering af, hvor meget kvanteinformation, der kan aflyttes
- Hydrogenbrændstof Vs. Fossil brændstof
- Quibi lancerer Hollywood på farten streaming under lockdown
- Snurrende, magnetiske mikrorobotter hjælper forskere med at undersøge genkendelse af immunceller


