Beregning af hydroniumionkoncentration [H3O+] ud fra pH - en trin-for-trin guide
Forstå forholdet
* pH er et mål for surhedsgraden eller alkaliniteten af en opløsning. Det er defineret som den negative logaritme (base 10) af hydroniumionkoncentrationen ([H3O+]).
* [H3O+] repræsenterer koncentrationen af hydroniumioner (H3O+) i mol pr. liter (mol/L).
Formlen
Forholdet mellem pH og [H3O+] er:
pH =-log[H3O+]
For at løse for [H3O+], skal vi omarrangere formlen:
[H3O+] =10^-pH
Beregning
1. Erstat den givne pH-værdi:
[H3O+] =10^-2,34
2. Beregn ved hjælp af en lommeregner:
[H3O+] ≈ 4,57 x 10^-3 mol/L
Derfor er H3O+-koncentrationen i en opløsning med en pH-værdi på 2,34 ca. 4,57 x 10^-3 mol/L.
 Varme artikler
Varme artikler
-
 Bioengineer har til formål at forvandle naturens virusbekæmpere til kraftfulde stofferKredit:CC0 Public Domain Blandt de kraftfulde biokemikalier i det menneskelige immunsystem, peptider er en af de bedste. Findes oftest på de steder, hvor mikrober elsker at slå rod - øjets slim
Bioengineer har til formål at forvandle naturens virusbekæmpere til kraftfulde stofferKredit:CC0 Public Domain Blandt de kraftfulde biokemikalier i det menneskelige immunsystem, peptider er en af de bedste. Findes oftest på de steder, hvor mikrober elsker at slå rod - øjets slim -
 Forskere udvikler en effektiv metode til at skabe højstyrkematerialer til fleksibel elektronikTPU-forskerne Raul David Rodriguez Contreras og Evgeniya Sheremet. Kredit:Tomsk Polytekniske Universitet TPU-forskere har sammen med deres kolleger fra udenlandske universiteter udviklet en metode
Forskere udvikler en effektiv metode til at skabe højstyrkematerialer til fleksibel elektronikTPU-forskerne Raul David Rodriguez Contreras og Evgeniya Sheremet. Kredit:Tomsk Polytekniske Universitet TPU-forskere har sammen med deres kolleger fra udenlandske universiteter udviklet en metode -
 Ramme for undersøgelse af ozonniveauer på realistiske indendørs overfladerGrafisk abstrakt. Kredit:Environmental Science &Technology (2022). DOI:10.1021/acs.est.1c08040 Et forskningssamarbejde ledet af Penn State havde til formål at forbedre forståelsen af indendørs oz
Ramme for undersøgelse af ozonniveauer på realistiske indendørs overfladerGrafisk abstrakt. Kredit:Environmental Science &Technology (2022). DOI:10.1021/acs.est.1c08040 Et forskningssamarbejde ledet af Penn State havde til formål at forbedre forståelsen af indendørs oz -
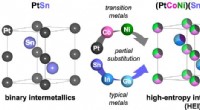 Carbonneutraliserende propylenproduktion katalyserer ændringer i petrokemisk teknikPlatin (Pt) og tin (Sn) steder i intermetallisk PtSn er delvist substitueret med henholdsvis Cobalt og nikkel (Co/Ni) og Indium og Gallium (In/Ga), hvilket danner en PtSn-type højentropi intermetallis
Carbonneutraliserende propylenproduktion katalyserer ændringer i petrokemisk teknikPlatin (Pt) og tin (Sn) steder i intermetallisk PtSn er delvist substitueret med henholdsvis Cobalt og nikkel (Co/Ni) og Indium og Gallium (In/Ga), hvilket danner en PtSn-type højentropi intermetallis
- Hvorfor eksploderer supernovaen ikke?
- Snap bønner svære at dyrke i dækafgrøderester
- Tesla udnævner ny bestyrelsesformand i forlig med regulatorer (opdatering)
- Videnskaben afslører, hvorfor ældre voksne udsender en mildt sød, muggen lugt
- Stanford-forskere ser fremtiden for solen, og det handler om nanodomes og plasmonics
- Er kvinder dårligere end mænd til lønforhandling?


