Molaritet vs. mol pr. liter:Forståelse af koncentrationsforskelle
Molaritet (M):
* Definition: Mol opløst stof pr. liter opløsning .
* Lydstyrke inkluderer: Både det opløste stof og opløsningsmidlet.
* Eksempel: En 1 M opløsning af NaCl indeholder 1 mol NaCl opløst i 1 liter opløsning.
Moler pr. liter opløsningsmiddel:
* Definition: Mol opløst stof pr. liter opløsningsmiddel .
* Lydstyrke inkluderer: Kun opløsningsmidlet.
* Eksempel: En 1 mol/L opløsning af NaCl indeholder 1 mol NaCl opløst i 1 liter vand (forudsat at vand er opløsningsmidlet).
Nøgleforskel:
Den største forskel er, at molaritet tager højde for opløsningens samlede volumen, mens mol pr. liter opløsningsmiddel kun tager højde for opløsningsmidlets volumen. Denne skelnen bliver væsentlig, når man har at gøre med opløsninger, hvor volumenændringen ved opløsning af det opløste stof er betydelig.
Hvornår skal du bruge hvilken:
* Molaritet foretrækkes generelt: Det er standardenheden til at udtrykke koncentration og bruges i vid udstrækning i kemiske reaktioner og beregninger.
* Moler pr. liter opløsningsmiddel kan være nyttige: Hvis du har brug for at kende koncentrationen af det opløste stof i form af volumen af opløsningsmiddel alene, er denne enhed passende. For eksempel i visse kemiske reaktioner, hvor volumenet af opløsningsmidlet er kritisk.
Opsummering:
Mens både molaritet og mol pr. liter opløsningsmiddel udtrykker koncentration, ligger forskellen i definitionen af det anvendte volumen. Molaritet tager højde for opløsningens samlede volumen, mens mol pr. liter opløsningsmiddel kun tager højde for opløsningsmidlets volumen. Vælg den passende enhed baseret på den specifikke kontekst for dit arbejde.
Sidste artikelBeregning af mol af NaCl:En trin-for-trin guide
Næste artikelBeregning af muldvarpe:Hvorfor molær masse alene ikke er nok
 Varme artikler
Varme artikler
-
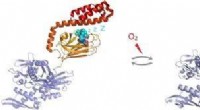 S-glutathionylering af human-inducerbar Hsp70 afslører reguleringsmekanisme, der involverer C-termi…Figur:Under oxidative stressforhold, den molekylære chaperon Hsp70 undergår post-translationel modifikation af cysteinrester ved tilsætning af tripeptidet glutathion. Glutathionylering inden for det s
S-glutathionylering af human-inducerbar Hsp70 afslører reguleringsmekanisme, der involverer C-termi…Figur:Under oxidative stressforhold, den molekylære chaperon Hsp70 undergår post-translationel modifikation af cysteinrester ved tilsætning af tripeptidet glutathion. Glutathionylering inden for det s -
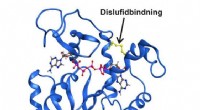 At få øje på det usynligeHøjopløsningsrøntgenstruktur af enzymet adenylatkinase fanget i en forbigående strukturel tilstand af en kovalent disulfidbinding. Kredit:Umeå Universitet Det er lykkedes kemikere ved Umeå Univers
At få øje på det usynligeHøjopløsningsrøntgenstruktur af enzymet adenylatkinase fanget i en forbigående strukturel tilstand af en kovalent disulfidbinding. Kredit:Umeå Universitet Det er lykkedes kemikere ved Umeå Univers -
 Processen fjerner samtidigt giftige metaller og salt for at producere rent vandEn fleksibel polymermembran, der indeholder nanopartikler af PAF, absorberer selektivt næsten 100% af metaller såsom kviksølv, kobber eller jern under afsaltning, mere effektivt at producere ren, sikk
Processen fjerner samtidigt giftige metaller og salt for at producere rent vandEn fleksibel polymermembran, der indeholder nanopartikler af PAF, absorberer selektivt næsten 100% af metaller såsom kviksølv, kobber eller jern under afsaltning, mere effektivt at producere ren, sikk -
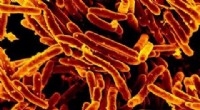 Forskere opdager en potentiel metode til at udsulte de bakterier, der forårsager tuberkuloseScanningselektronmikrofotografi af Mycobacterium tuberculosis bakterier, som forårsager TB. Kredit:NIAID Infektionssygdommen tuberkulose (TB) er en af de førende dødsårsager på verdensplan. Mens
Forskere opdager en potentiel metode til at udsulte de bakterier, der forårsager tuberkuloseScanningselektronmikrofotografi af Mycobacterium tuberculosis bakterier, som forårsager TB. Kredit:NIAID Infektionssygdommen tuberkulose (TB) er en af de førende dødsårsager på verdensplan. Mens
- Har Facebook-data hjulpet Trump? Great Hack udforsker skandale
- Hvilken reproduktionsstruktur hos kvinder indeholder erektil væv?
- Hvad er en atmosfærefølende enhed?
- Nanovidenskab giver indsigt i verdens mindste økosystemer
- Undersøgelse afslører personlighedsændringer i ungarske premierministres talemønstre
- Forskning fremhæver de økonomiske omkostninger ved mobning på arbejdspladsen


