Silicium-oxygenbindingspolaritet:Forståelse af elektronegativitet og ladningsfordeling
* Elektronegativitetsforskel: Ilt er meget mere elektronegativt end silicium. Det betyder, at oxygen har en stærkere tiltrækning af de fælles elektroner i bindingen.
* Electron Density Shift: De delte elektroner i Si-O-bindingen bruger mere tid tættere på oxygenatomet. Dette skaber en delvis negativ ladning (δ-) på oxygenatomet og en delvis positiv ladning (δ+) på siliciumatomet.
* Polær tegn: Den ulige deling af elektroner og de resulterende partielle ladninger giver Si-O-bindingen dens polære karakter.
Denne polaritet har betydelige konsekvenser for egenskaberne af siliciumdioxid (SiO2), som er den primære bestanddel af glas og sand:
* Højt smeltepunkt: De stærke polære bindinger skaber en stærk netværksstruktur, hvilket fører til et højt smeltepunkt.
* Isolerende egenskaber: Den polære natur bidrager til, at SiO2 er en fremragende isolator, hvilket gør den anvendelig i elektronik.
* Opløselighed: De polære bindinger tillader SiO2 at opløses i stærke syrer og baser.
Samlet set spiller den polære natur af Si-O-bindingen en afgørende rolle i bestemmelsen af de fysiske og kemiske egenskaber af siliciumdioxid og mange andre siliciumforbindelser.
 Varme artikler
Varme artikler
-
 Forskere finder en måde at udnytte hele spektret af sollysForskere har vist, for første gang, at det er muligt at indsamle energi fra hele det synlige spektrum af sollys og transformere det, hurtigt og effektivt, til brint som brændstof. Kredit:David Monje p
Forskere finder en måde at udnytte hele spektret af sollysForskere har vist, for første gang, at det er muligt at indsamle energi fra hele det synlige spektrum af sollys og transformere det, hurtigt og effektivt, til brint som brændstof. Kredit:David Monje p -
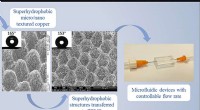 Ny fremstillingsproces skaber supersmå kanaler til at afvise vand og forbedre medicinsk, elektronis…Dette billede viser skabelsen af en superhydrofob overflade på en metaloverflade med en ultrahurtig laser, som overføres til PMDS via transferstøbning og samles til en mikrofluidisk enhed. Kredit:Pu
Ny fremstillingsproces skaber supersmå kanaler til at afvise vand og forbedre medicinsk, elektronis…Dette billede viser skabelsen af en superhydrofob overflade på en metaloverflade med en ultrahurtig laser, som overføres til PMDS via transferstøbning og samles til en mikrofluidisk enhed. Kredit:Pu -
 Sådan opdager du en kemisk ændring:5 klare indikatorerAf Riti Gupta | Opdateret 30. august 2022 Ivan-balvan/iStock/GettyImages Mens de individuelle atomer og molekyler, der er involveret i en kemisk ændring, normalt er usynlige, efterlader mange reakti
Sådan opdager du en kemisk ændring:5 klare indikatorerAf Riti Gupta | Opdateret 30. august 2022 Ivan-balvan/iStock/GettyImages Mens de individuelle atomer og molekyler, der er involveret i en kemisk ændring, normalt er usynlige, efterlader mange reakti -
 Undersøgelse udvider, hvad vi ved om naturlige, billige måder at fjerne forurenende stoffer fra va…Inden for timer, tørrede og malede avocadoskaller hjælper med at fjerne methylenblåt farvestof fra vand gennem en proces, der kaldes adsorption. Kredit:Dickinson College Nypubliceret forskning fra
Undersøgelse udvider, hvad vi ved om naturlige, billige måder at fjerne forurenende stoffer fra va…Inden for timer, tørrede og malede avocadoskaller hjælper med at fjerne methylenblåt farvestof fra vand gennem en proces, der kaldes adsorption. Kredit:Dickinson College Nypubliceret forskning fra
- Er den carnelianske rock stødende metamorfe eller sedimentære?
- Sætter mikroskopet på mediedækning for Stillehavsarbejdere
- Har træer høje tykke og træagtige stængler?
- At komme til bunden af arktiske jordskred
- Omarrangering i Meiose:Hvordan kromosomal krydsning driver genetisk mangfoldighed
- Hvordan man laver en Popcorn Science Fair Project


