Kovalente vs. ioniske bindinger i siliciumforbindelser:en forklaring
* Elektronegativitet: Silicium har en elektronegativitet på 1,9, mens oxygen (et almindeligt grundstof i siliciumforbindelser) har en elektronegativitet på 3,5. Denne forskel i elektronegativitet er signifikant, men ikke stor nok til at danne en virkelig ionbinding.
* Bindende tegn: Bindingen i siliciumforbindelser beskrives ofte som polær kovalent , hvilket betyder, at elektronerne deles ulige mellem silicium og andre atomer. Dette skyldes elektronegativitetsforskellen, som resulterer i en delvis negativ ladning på det mere elektronegative atom og en delvis positiv ladning på siliciumatomet.
* Eksempler: Almindelige siliciumforbindelser som siliciumdioxid (SiO2) og siliciumcarbid (SiC) betragtes begge som kovalente forbindelser.
Vigtig bemærkning: Der er nogle siliciumforbindelser, der udviser en vis ionisk karakter, især når de er bundet med stærkt elektronegative elementer som fluor (f.eks. SiF4). Imidlertid er størstedelen af siliciumforbindelserne overvejende kovalente.
 Varme artikler
Varme artikler
-
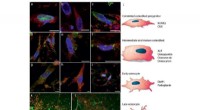 Forskere dyrker den mest naturtro knogle endnu fra vævede cellerDifferentiering af hBMSCer til osteoblaster og osteocytter:a–i) Fluorescensimmunhistokemi billeddannelse, der viser markører for a–c) tidlige stadier af osteoblastdannelse, d–f) modne osteoblaster, og
Forskere dyrker den mest naturtro knogle endnu fra vævede cellerDifferentiering af hBMSCer til osteoblaster og osteocytter:a–i) Fluorescensimmunhistokemi billeddannelse, der viser markører for a–c) tidlige stadier af osteoblastdannelse, d–f) modne osteoblaster, og -
 Ny algoritme giver mulighed for hurtigere, dyrefri kemisk toksicitetstestKredit:CC0 Public Domain Brugen af dyr til at teste kemikaliers toksicitet kan en dag blive forældet takket være en lav pris, højhastighedsalgoritme udviklet af forskere ved Rutgers og andre uni
Ny algoritme giver mulighed for hurtigere, dyrefri kemisk toksicitetstestKredit:CC0 Public Domain Brugen af dyr til at teste kemikaliers toksicitet kan en dag blive forældet takket være en lav pris, højhastighedsalgoritme udviklet af forskere ved Rutgers og andre uni -
 Nyt materiale til at overgå traditionelle oxygenreduktionsreaktionskatalysatorerKredit:CC0 Public Domain En forskergruppe ledet af prof. YANG Minghui ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under det kinesiske videnskabsakademi (CAS) opdagede, at
Nyt materiale til at overgå traditionelle oxygenreduktionsreaktionskatalysatorerKredit:CC0 Public Domain En forskergruppe ledet af prof. YANG Minghui ved Ningbo Institute of Materials Technology and Engineering (NIMTE) under det kinesiske videnskabsakademi (CAS) opdagede, at -
 Bioaktive naturlige forbindelser til kampen mod kræftSojaplanter producerer glyceolliner som reaktion på patogenangreb såsom svampe, bakterier eller UV-bestråling, for at bevare deres helbred. Kredit:pixabay.com Phytoalexiner er bioaktive fytokemika
Bioaktive naturlige forbindelser til kampen mod kræftSojaplanter producerer glyceolliner som reaktion på patogenangreb såsom svampe, bakterier eller UV-bestråling, for at bevare deres helbred. Kredit:pixabay.com Phytoalexiner er bioaktive fytokemika
- Hvilken region, der producerer celler i en plante?
- Hvor mange Apollo -fly var der?
- Forskere udvikler genforarbejdelige termohærder til bæredygtig 3-D-print
- Er voldelige eksplosioner fra solflekker, hvor gas og enorme mængder energi sprænges i rummet væk…
- Hvorfor betragtes bakterier ikke -levende?
- Hvad involverer bevægelse af materialer inde i celle såvel mellem dele en multicellulær organisme…


