Forstå kræfterne, der holder flydende nitrogen sammen
Her er en opdeling:
* Nitrogen er et ikke-polært molekyle: Nitrogengas (N2) består af to nitrogenatomer, der er tredobbeltbundet til hinanden. Denne stærke binding skaber et symmetrisk molekyle uden permanent dipolmoment.
* Van der Waals styrker: Disse er svage, midlertidige tiltrækningskræfter, der opstår fra den konstante bevægelse af elektroner i molekyler.
* Spredningskræfter i London: Disse er den svageste type van der Waals-kraft, der forekommer mellem alle molekyler, selv ikke-polære. De opstår fra midlertidige, øjeblikkelige dipoler induceret i molekylernes elektronskyer på grund af elektronernes tilfældige bevægelse.
Sådan virker det:
1. Midlertidige dipoler: Når elektroner bevæger sig rundt i nitrogenmolekylet, kan de skabe flygtige øjeblikke, hvor den ene ende af molekylet bliver lidt mere negativ og den anden ende lidt mere positiv.
2. Attraktion: Disse midlertidige dipoler inducerer midlertidige dipoler i tilstødende nitrogenmolekyler. De modsatte ladninger af disse midlertidige dipoler tiltrækker så hinanden og holder molekylerne sammen.
Vigtige punkter:
* Svage kræfter: Selvom disse kræfter er svage individuelt, er den kumulative effekt af mange London-spredningskræfter nok til at holde flydende nitrogen sammen ved lave temperaturer.
* Lavt kogepunkt: Svagheden af disse kræfter forklarer, hvorfor nitrogen har et meget lavt kogepunkt (-195,8 °C) - den termiske energi ved højere temperaturer overvinder de kræfter, der holder væsken sammen.
Opsummering: Flydende nitrogen holdes sammen af midlertidige, svage attraktioner kendt som London-spredningskræfter, som opstår fra de midlertidige dipoler induceret i nitrogenmolekylernes elektronskyer på grund af tilfældig elektronbevægelse.
 Varme artikler
Varme artikler
-
 Smeltning af skrottede enheder, da bæredygtige behov opvarmesKredit:University of Queensland Smeltning af metaller fra kasserede elektroniske enheder er blandt løsninger til bæredygtig forsyning af kritiske materialer, der undersøges af forskere fra Univers
Smeltning af skrottede enheder, da bæredygtige behov opvarmesKredit:University of Queensland Smeltning af metaller fra kasserede elektroniske enheder er blandt løsninger til bæredygtig forsyning af kritiske materialer, der undersøges af forskere fra Univers -
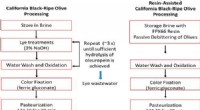 En grønnere måde at tage bitterheden ud af olivenKredit:American Chemical Society Oliven er en del af middelhavskosten, som har været forbundet med en reduceret forekomst af hjerte-kar-sygdomme, Alzheimers sygdom og andre tilstande. Imidlertid,
En grønnere måde at tage bitterheden ud af olivenKredit:American Chemical Society Oliven er en del af middelhavskosten, som har været forbundet med en reduceret forekomst af hjerte-kar-sygdomme, Alzheimers sygdom og andre tilstande. Imidlertid, -
 Ozon nedbryder THC aflejret på overflader fra tredjehånds cannabisrøgKredit:CC0 Public Domain Anden og tredjehånds tobaksrøg har fået masser af opmærksomhed, men meget mindre er kendt om de forbindelser, der aflejres på overflader fra cannabisrøg. Nu, forskere, der
Ozon nedbryder THC aflejret på overflader fra tredjehånds cannabisrøgKredit:CC0 Public Domain Anden og tredjehånds tobaksrøg har fået masser af opmærksomhed, men meget mindre er kendt om de forbindelser, der aflejres på overflader fra cannabisrøg. Nu, forskere, der -
 Forskere designer ny metabolisk teknologi for at åbne videnskabelige data for alleKredit:CC0 Public Domain Patienter ønsker at se deres medicinske oplysninger. Forskere vil gerne dele deres data. Nu, forskere ved Scripps Research har frigivet en ny teknologi designet til at gø
Forskere designer ny metabolisk teknologi for at åbne videnskabelige data for alleKredit:CC0 Public Domain Patienter ønsker at se deres medicinske oplysninger. Forskere vil gerne dele deres data. Nu, forskere ved Scripps Research har frigivet en ny teknologi designet til at gø


