Zink i natriumhydroxid:reaktion, produkter og observationer
Zn(s) + 2NaOH(aq) + 2H2O(l) → Na2[Zn(OH)4](aq) + H2(g)
Her er en opdeling:
* Zink (Zn) reagerer med natriumhydroxid (NaOH) i nærvær af vand (H2O) .
* Reaktionen producerer natriumtetrahydroxozincat(II) (Na₂[Zn(OH)4]) , en opløselig kompleks ion og hydrogengas (H2) .
Observationer:
* Du vil se bobler af brintgas udvikle sig fra opløsningen.
* Zinkmetallet vil opløses, og opløsningen bliver klar.
* Opløsningen vil være let basisk på grund af tilstedeværelsen af hydroxidioner.
Vigtige bemærkninger:
* Denne reaktion er et eksempel på en redoxreaktion. Zink oxideres (taber elektroner) til dannelse af Zn²⁺-ioner, mens hydrogenioner i vand reduceres (vinder elektroner) for at danne brintgas.
* Reaktionen begunstiges i nærværelse af overskydende hydroxidioner. Dette skyldes, at dannelsen af tetrahydroxozincat(II)-kompleksionen fjerner zinkioner fra opløsningen, hvilket driver reaktionen fremad.
Sig til, hvis du gerne vil vide mere om reaktionen eller nogle af de dannede produkter!
Sidste artikelForståelse af ionisering:Hvad sker der, når syrer opløses?
Næste artikelSaltsyre og fordøjelse:Hvordan det nedbryder mad
 Varme artikler
Varme artikler
-
 Maskinlæring forudsiger mekaniske egenskaber af porøse materialerKrystallinsk metal-organisk ramme. Kredit:David Fairen-Jimenez Maskinlæring kan bruges til at forudsige egenskaberne af en gruppe materialer, som, ifølge nogle, kunne være lige så vigtig for det 2
Maskinlæring forudsiger mekaniske egenskaber af porøse materialerKrystallinsk metal-organisk ramme. Kredit:David Fairen-Jimenez Maskinlæring kan bruges til at forudsige egenskaberne af en gruppe materialer, som, ifølge nogle, kunne være lige så vigtig for det 2 -
 Forskere rapporterer om cellegennemtrængelige nanobodiesRingpeptider åbner cellemembrandøren og tillader antistoffer og andre terapeutiske midler at trænge ind i cellerne. Kredit:Christoph Hohmann, Nanosystems Initiative München (NIM) Forskere ved Tech
Forskere rapporterer om cellegennemtrængelige nanobodiesRingpeptider åbner cellemembrandøren og tillader antistoffer og andre terapeutiske midler at trænge ind i cellerne. Kredit:Christoph Hohmann, Nanosystems Initiative München (NIM) Forskere ved Tech -
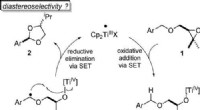 Forskere udvikler en bæredygtig katalyseprocesAtomøkonomisk omdannelse af benzylethere til acetaler ved titanocen(III)-katalyse i enkeltelektrontrin (SET). Angewandte Chemie, DOI:10.1002/anie.202013561 Acetaler er vigtige kemiske forbindelser
Forskere udvikler en bæredygtig katalyseprocesAtomøkonomisk omdannelse af benzylethere til acetaler ved titanocen(III)-katalyse i enkeltelektrontrin (SET). Angewandte Chemie, DOI:10.1002/anie.202013561 Acetaler er vigtige kemiske forbindelser -
 Trin-for-trin guide:Syntetisering af sølvoxid fra sølvnitratAf Alec Tasi | Opdateret 30. august 2022 Mens sølvs metalliske glans er dens mest berømte egenskab, er dens kemi lige så fascinerende. Et af de mest almindelige laboratoriepræparater involverer omdan
Trin-for-trin guide:Syntetisering af sølvoxid fra sølvnitratAf Alec Tasi | Opdateret 30. august 2022 Mens sølvs metalliske glans er dens mest berømte egenskab, er dens kemi lige så fascinerende. Et af de mest almindelige laboratoriepræparater involverer omdan
- Hvad er to måder, min krop bruger fødevareenergi på?
- Hvad er 5 levende dele af et økosystem?
- Hvilket element kommer dioxid fra?
- 1+ ioner:Identifikation af grundstoffer og eksempler - kemi forklaret
- Undersøgelse lokaliserer oprindelsen af gletsjersodforurening i det nordlige Indien
- Slyngelplaneter kan være flere end stjernerne


