Forståelse af entalpi og entropiændring i kemiske reaktioner
* ΔH =62,4 kJ/mol :Dette indikerer, at reaktionen er endoterm . En positiv entalpiændring betyder, at reaktionen absorberer varme fra omgivelserne.
* ΔS =0,145 kJ/mol K :Dette indikerer, at reaktionen har en lille stigning i entropi . En positiv entropiændring betyder, at reaktionen fører til en mere uordnet tilstand.
Samlet analyse:
Reaktionen er endoterm (kræver varme) og har en lille stigning i entropi. Dette betyder, at reaktionen ikke er spontan under standardbetingelser .
Her er grunden:
* Spontanitet af en reaktion bestemmes af Gibbs frie energiændring (ΔG).
* ΔG =ΔH - TΔS
* For en spontan reaktion skal ΔG være negativ.
Da ΔH er positiv (endotermisk) og ΔS er lille og positiv, ved standardtemperaturer (typisk omkring 298 K), vil værdien af ΔG sandsynligvis være positiv. Dette indikerer, at reaktionen er ikke-spontan under standardbetingelser.
Vigtig bemærkning:
* Temperaturen spiller en afgørende rolle. Selvom reaktionen er ikke-spontan ved standardbetingelser, kan den blive spontan ved højere temperaturer. Dette skyldes, at TΔS-leddet i Gibbs fri energiligning bliver større, når temperaturen stiger.
Opsummering: Baseret på de angivne oplysninger er reaktionen sandsynligvis ikke-spontan under standardbetingelser. Det kan dog blive spontant ved højere temperaturer.
 Varme artikler
Varme artikler
-
 Hurtigkøling:Afkøl sodavandsdåser med saltet isvandAf Pearl Lewis Opdateret 24. marts 2022 Udnytter det samme princip, som en mættet saltvandsopslæmning, når den først er født, kan sænke temperaturen under det normale frysepunkt for vand - helt ned
Hurtigkøling:Afkøl sodavandsdåser med saltet isvandAf Pearl Lewis Opdateret 24. marts 2022 Udnytter det samme princip, som en mættet saltvandsopslæmning, når den først er født, kan sænke temperaturen under det normale frysepunkt for vand - helt ned -
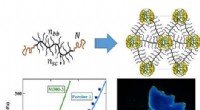 Polymerer, der efterligner kamæleons hudØverst til venstre:molekylær struktur af en plastomer syntetiseret i dette værk; højre:supramolekylær struktur dannet ved samling af identiske plastomerer. Nederst-til venstre:belastningskurver til pl
Polymerer, der efterligner kamæleons hudØverst til venstre:molekylær struktur af en plastomer syntetiseret i dette værk; højre:supramolekylær struktur dannet ved samling af identiske plastomerer. Nederst-til venstre:belastningskurver til pl -
 Flow kemi teknik tilbyder hurtigere, sikrere måde at skærme på, studere og optimere industrielle …Forskere har udviklet en flowbaseret high-throughput screening teknologi, der tilbyder en hurtigere, sikrere og billigere midler til at identificere optimale betingelser for at udføre katalytiske kemi
Flow kemi teknik tilbyder hurtigere, sikrere måde at skærme på, studere og optimere industrielle …Forskere har udviklet en flowbaseret high-throughput screening teknologi, der tilbyder en hurtigere, sikrere og billigere midler til at identificere optimale betingelser for at udføre katalytiske kemi -
 Titrering forklaret:Hvordan kemikere måler ukendte koncentrationerTitrering er en hjørnestensanalyseteknik, der bruges i kemilaboratorier over hele verden. Studerende udfører typisk mindst én syre-base titrering før eksamen, med phenolphtalein som den mest almindeli
Titrering forklaret:Hvordan kemikere måler ukendte koncentrationerTitrering er en hjørnestensanalyseteknik, der bruges i kemilaboratorier over hele verden. Studerende udfører typisk mindst én syre-base titrering før eksamen, med phenolphtalein som den mest almindeli
- En optimeret struktur af memristiv enhed til neuromorfe computersystemer
- UA-opfundet solcreme licenseret til førende aloe vera-leverandør
- Archaeal enzym, der producerer membranlipider, er spektakulært promiskuøst
- Hvilken proces ændrer væske til gas?
- Forskeren bruger Westminster Abbey -vinduer til at skinne lys over glasmyten
- Hvordan ændrer højde den potentielle energi fra et objekt?


