Termokemiske tegnkonvention:Forståelse af varmeflow
* Varme absorberet af systemet: Positiv (+)
* Varme frigivet af systemet: Negativ (-)
Her er en oversigt:
System: Systemet refererer til den specifikke del af universet, du studerer, som en kemisk reaktion.
Omgivelser: Omgivelserne er alt andet uden for systemet.
Varmeflow: Der kan strømme varme mellem systemet og omgivelserne.
Endoterm reaktion: En reaktion, der absorberer varme fra omgivelserne. Systemet får energi, og entalpiændringen (ΔH) er positiv .
Eksoterm reaktion: En reaktion, der frigiver varme til omgivelserne. Systemet mister energi, og entalpiændringen (ΔH) er negativ .
Eksempler:
* Smeltende is: Isen optager varme fra omgivelserne og bliver til flydende vand. Dette er en endoterm proces, ΔH> 0.
* Brændstof: Det brændende brændstof afgiver varme til omgivelserne. Dette er en eksoterm proces, ΔH <0.
Vigtig bemærkning: Denne konvention er bredt accepteret i kemi, men det er afgørende at kontrollere den specifikke kontekst af enhver termokemisk beregning for at bekræfte den konvention, der bruges.
 Varme artikler
Varme artikler
-
 En hurtig, en miljøvenlig måde at afise fly påEt nærbillede af NACA-flyveprofilens overflade taget fra oven. Det blev funktionaliseret ved hjælp af DLIP. Kredit:Airbus Is på et flys overflade kan være en fare. Det øger luftmodstand og brændst
En hurtig, en miljøvenlig måde at afise fly påEt nærbillede af NACA-flyveprofilens overflade taget fra oven. Det blev funktionaliseret ved hjælp af DLIP. Kredit:Airbus Is på et flys overflade kan være en fare. Det øger luftmodstand og brændst -
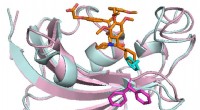 Depression, fedme, kroniske smerter kan behandles ved at målrette det samme nøgleproteinEn ny inhibitor (orange) er selektiv for FKBP51, som er involveret i depression, kroniske smerter og fedme. Kredit:Felix Hausch Større depression, fedme og kronisk smerte er alle forbundet med vir
Depression, fedme, kroniske smerter kan behandles ved at målrette det samme nøgleproteinEn ny inhibitor (orange) er selektiv for FKBP51, som er involveret i depression, kroniske smerter og fedme. Kredit:Felix Hausch Større depression, fedme og kronisk smerte er alle forbundet med vir -
 Et levende lys-lignende skær fra en fleksibel organisk LEDEn bøjelig organisk LED med en naturlig glimmerbagside frigiver en stærk, levende lys-lignende glød. Kredit:Andy Chen og Ambrose Chen Stearinlys giver en behagelig glød og sætter stemningen til en
Et levende lys-lignende skær fra en fleksibel organisk LEDEn bøjelig organisk LED med en naturlig glimmerbagside frigiver en stærk, levende lys-lignende glød. Kredit:Andy Chen og Ambrose Chen Stearinlys giver en behagelig glød og sætter stemningen til en -
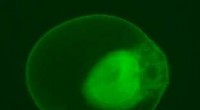 Enzymdrevne protoceller stiger til toppenFluorescensmikroskopibillede af en enzymholdig protocelle samlet af en blanding af DNA og lerpartikler. Kredit:Professor Stephen Mann, University of Bristol Forskere ved University of Bristol har
Enzymdrevne protoceller stiger til toppenFluorescensmikroskopibillede af en enzymholdig protocelle samlet af en blanding af DNA og lerpartikler. Kredit:Professor Stephen Mann, University of Bristol Forskere ved University of Bristol har
- Nyt materiale sænker energiforbruget i forbindelse med ethylenproduktion
- Hvilken type energibutikker energi?
- Designer nanozymer til reaktive iltarter, der fjerner antiinflammatorisk terapi
- Hvorfor er Brazils vådområder opslugt af flammer?
- Hvilken energi konverteres, når du cykler?
- Hvor mange tons CO2 i 1 kWh?


