Natrium- og kuldioxidreaktion:risici og farer
* Reaktivitet: Natrium er et meget reaktivt alkalimetal. Den reagerer voldsomt med vand og endda med fugten i luften. Kuldioxid, selvom det ikke er iboende reaktivt med natrium, findes ofte i miljøer, hvor fugt er til stede.
* Eksoterm reaktion: Reaktionen mellem natrium og kuldioxid er eksoterm, hvilket betyder, at den frigiver varme. Denne varme kan få natriumet til at antænde og brænde.
* Brandfare: Det brændende natrium vil producere en lys gul flamme og en masse røg. Denne røg kan være irriterende og giftig.
* Eksplosionspotentiale: Hvis reaktionen sker i et lukket rum, kan trykopbygningen fra de frigjorte gasser føre til en eksplosion.
I stedet for at blande dem direkte er her, hvad der kan ske afhængigt af de specifikke forhold:
* I nærvær af fugt: Natriumet vil reagere voldsomt med vand, danne natriumhydroxid (NaOH) og frigive brintgas (H2). Denne reaktion er meget eksoterm og kan forårsage antændelse. Kuldioxiden kunne derefter reagere med natriumhydroxidet og danne natriumbicarbonat (NaHCO3).
* Under kontrollerede forhold: Natrium og kuldioxid kan reageres under kontrollerede forhold i laboratoriemiljøer til fremstilling af natriumcarbonat (Na2CO3). Denne reaktion kræver specifikke temperatur- og trykparametre.
Som konklusion: At blande natrium og kuldioxid direkte er utroligt farligt og bør undgås. Hvis du skal bruge natrium, skal du sørge for, at det håndteres i et sikkert og kontrolleret miljø.
Sidste artikelIonisk ligevægt forklaret:Forståelse af dissociation og balance
Næste artikelBrintforbrænding:Hvad dannes, når brint brænder?
 Varme artikler
Varme artikler
-
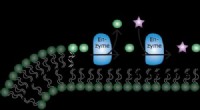 Archaeal enzym, der producerer membranlipider, er spektakulært promiskuøstIllustrationen viser produktionen af forskellige cardiolipiner og fosfolipider ved inkorporering af miljøforbindelser som lipidhovedgruppe. Kredit:Marten Exterkate, Universitetet i Groningen Cel
Archaeal enzym, der producerer membranlipider, er spektakulært promiskuøstIllustrationen viser produktionen af forskellige cardiolipiner og fosfolipider ved inkorporering af miljøforbindelser som lipidhovedgruppe. Kredit:Marten Exterkate, Universitetet i Groningen Cel -
 Forskere foreslår ny tilgang til måling af atomerForsiden illustrerer effekten af geometribaseret filtrering af intermolekylære kontakter på deres afstandsfordeling. Linje-of-sight-princippet eliminerer effektivt baggrunden for tilfældigt fordelte
Forskere foreslår ny tilgang til måling af atomerForsiden illustrerer effekten af geometribaseret filtrering af intermolekylære kontakter på deres afstandsfordeling. Linje-of-sight-princippet eliminerer effektivt baggrunden for tilfældigt fordelte -
 Når livet giver dig citroner, lave bioplastLimonen kan være nøglen til nye, miljøvenlige polymerer. Kredit:Public domain Fra dit telefoncover til flyvinduer, polycarbonater er overalt. Flere millioner tons polycarbonat produceres hvert år
Når livet giver dig citroner, lave bioplastLimonen kan være nøglen til nye, miljøvenlige polymerer. Kredit:Public domain Fra dit telefoncover til flyvinduer, polycarbonater er overalt. Flere millioner tons polycarbonat produceres hvert år -
 Laboratorietest viser, at molekyle ser ud til at anspore til celledød i tumorer, betændelseEt lægemiddellignende molekyle udviklet af Duke Health-forskere ser ud til at gå i forbøn for en inflammatorisk reaktion, der er i centrum for en række forskellige sygdomme. Kredit:Duke Health Et
Laboratorietest viser, at molekyle ser ud til at anspore til celledød i tumorer, betændelseEt lægemiddellignende molekyle udviklet af Duke Health-forskere ser ud til at gå i forbøn for en inflammatorisk reaktion, der er i centrum for en række forskellige sygdomme. Kredit:Duke Health Et
- Påvirker det at bo i nærheden af vindmøller menneskers sundhed negativt?
- Hvad sker der, når kobber reagerer med nitinsyre?
- Hvordan hjælper det at redde energi verden?
- Er der en ny planet med ringe?
- Hvorfor er salt værdifuldt i regnskoven?
- New Delhi sælger hele ejerandelen i det gældsplagede Air India


