Ionisk ligevægt forklaret:Forståelse af dissociation og balance
Ionisk ligevægt:En balancegang i løsninger
Ionisk ligevægt beskriver den dynamiske balancetilstand mellem ioner i en løsning. Det er som et tovtrækkeri mellem opløste ioner og deres tendens til at omdannes til neutrale forbindelser. Denne ligevægt ændrer sig konstant, med ioner, der konstant dissocierer og rekombinerer.
Her er en oversigt over de vigtigste aspekter:
1. Spillerne:
* Elektrolytter: Stoffer, der producerer ioner, når de opløses i vand. De kan være:
* Stærke elektrolytter: Dissocier fuldstændigt til ioner (f.eks. stærke syrer, stærke baser, salte).
* Svage elektrolytter: Dissocierer delvist til ioner (f.eks. svage syrer, svage baser).
* ioner: Ladede partikler dannet af forstærkning eller tab af elektroner.
2. Ligevægten:
* Dissociation: Processen, hvor elektrolytter bryder sammen til ioner i opløsning.
* Forening: Processen, hvor ioner rekombinerer for at danne neutrale forbindelser.
* Ligevægt: Den tilstand, hvor hastighederne for dissociation og association er ens, hvilket fører til en konstant koncentration af ioner.
3. Nøglebegreber:
* Opløselighedsprodukt (Ksp): Repræsenterer det omfang, i hvilket en let opløselig ionforbindelse opløses. Det er produktet af ionkoncentrationer ved ligevægt.
* Ioniseringskonstant (Ka/Kb): Måler i hvilket omfang en svag syre eller base dissocierer. Det er forholdet mellem produktkoncentrationer og reaktantkoncentrationer ved ligevægt.
* Almindelig ioneffekt: Faldet i opløselighed af et let opløseligt salt, når et opløseligt salt indeholdende en fælles ion tilsættes opløsningen.
* Bufferløsninger: Opløsninger, der modstår ændringer i pH ved tilsætning af syre eller base. De indeholder en svag syre og dens konjugerede base (eller en svag base og dens konjugerede syre) i betydelige koncentrationer.
4. Betydningen af ionisk ligevægt:
* Kemiske reaktioner: Mange reaktioner i opløsning afhænger af koncentrationen af specifikke ioner.
* Opløselighed: Forståelse af ionisk ligevægt hjælper med at forudsige opløseligheden af ioniske forbindelser.
* Biologiske systemer: Ionisk ligevægt spiller en afgørende rolle i biologiske processer som blodets pH-regulering, enzymaktivitet og nerveimpulstransmission.
* Miljøvidenskab: Forståelse af ionisk ligevægt er vigtig for at studere vandkvalitet, forurening og afhjælpning.
I bund og grund styrer ionisk ligevægt adfærden af ioner i opløsninger, hvilket påvirker forskellige kemiske og biologiske processer.
Fortæl mig, hvis du gerne vil udforske nogle af disse begreber mere detaljeret!
Sidste artikelCobalt(II) Nitrat (Co(NO3)2):Formel og nomenklatur
Næste artikelNatrium- og kuldioxidreaktion:risici og farer
 Varme artikler
Varme artikler
-
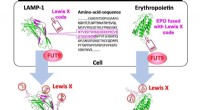 Forskerhold identificerer en molekylær kode indlejret i protein til regulering af dets glykosylerin…Specifik 29-aminosyresekvens fra LAMP-1 tjener som en Lewis X-kode, som dechifreres af FUT9, og den kan indlejres i erythropoietin for at fremkalde Lewis X-modifikation. Kredit:Nagoya City University
Forskerhold identificerer en molekylær kode indlejret i protein til regulering af dets glykosylerin…Specifik 29-aminosyresekvens fra LAMP-1 tjener som en Lewis X-kode, som dechifreres af FUT9, og den kan indlejres i erythropoietin for at fremkalde Lewis X-modifikation. Kredit:Nagoya City University -
 Mikrobielt tyveri muliggør nedbrydning af metan, giftig methylkviksølvForskere fik ny indsigt i de mekanismer, som nogle methan-fødende bakterier kaldet metanotrofer bruger til at nedbryde toksinet methylkviksølv. Kredit:Andy Sproles/ORNL, US Department of Energy; Jerem
Mikrobielt tyveri muliggør nedbrydning af metan, giftig methylkviksølvForskere fik ny indsigt i de mekanismer, som nogle methan-fødende bakterier kaldet metanotrofer bruger til at nedbryde toksinet methylkviksølv. Kredit:Andy Sproles/ORNL, US Department of Energy; Jerem -
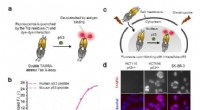 Forskere rapporterer om levende intracellulær billeddannelse med ny, betinget aktiv immunfluorescen…(a) Det dobbeltmærkede fluorescerende farvestof i det antigenfragmentbaserede Q-legeme dequenches ved binding med målantigenet og viser således fluorescerende signalering til visualisering af det intr
Forskere rapporterer om levende intracellulær billeddannelse med ny, betinget aktiv immunfluorescen…(a) Det dobbeltmærkede fluorescerende farvestof i det antigenfragmentbaserede Q-legeme dequenches ved binding med målantigenet og viser således fluorescerende signalering til visualisering af det intr -
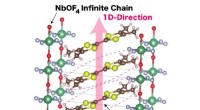 Forskere opdager ny organisk lederKrystalstruktur af en-dimensionel ladningsoverføringssalt med en uendelig anionkæde (TMTTF) (NbOF 4 ) Kredit:NINS/IMS Salte er langt mere komplicerede end fødevarekrydderiet - de kan endda funge
Forskere opdager ny organisk lederKrystalstruktur af en-dimensionel ladningsoverføringssalt med en uendelig anionkæde (TMTTF) (NbOF 4 ) Kredit:NINS/IMS Salte er langt mere komplicerede end fødevarekrydderiet - de kan endda funge
- Automatisering har potentialet til at forbedre ligestilling mellem kønnene på arbejdspladsen
- Ionbindinger:Styrke og sammenligning med andre kemiske bindinger
- Hvilken type energi et objekt har, når den holdes 1 meter over jorden?
- Hvide blodlegemer:funktioner og immunforsvar forklaret
- Fremtidige oversvømmelser af Brahmaputra-floden, da klimaændringer kan blive undervurderet, siger …
- S-t-r-e-t-c-h-i-n-g elektrisk konduktans til grænsen


