Fordampningsvarme:Hvorfor diethylether kræver mindre energi end ethanol
1. Intermolekylære kræfter:
* Ethanol (CH3CH2OH): Ethanol danner hydrogenbindinger. Disse er stærke intermolekylære kræfter på grund af hydrogenatomet direkte bundet til et oxygenatom. Hydrogenbindinger kræver en betydelig mængde energi for at bryde, hvilket fører til en højere fordampningsentalpi.
* Diethylether (CH3CH2OCH2CH3): Diethylether oplever primært dipol-dipol-interaktioner og London-spredningskræfter. Disse er svagere end hydrogenbindinger.
2. Molekylær struktur:
* Ethanol: Tilstedeværelsen af hydroxylgruppen (-OH) i ethanol muliggør hydrogenbinding, hvilket bidrager til dens højere kogepunkt og fordampningsentalpi.
* Diethylether: Den etherfunktionelle gruppe (R-O-R) mangler hydrogenbindingsevnen til stede i ethanol.
3. Entalpi af fordampning:
Fordampningsentalpien er den mængde energi, der kræves for at fordampe et mol af et stof ved dets kogepunkt. Da diethylether oplever svagere intermolekylære kræfter, er mindre energi nødvendig for at bryde disse interaktioner og overføre molekylerne fra væske til gas.
Opsummering:
De svagere intermolekylære kræfter i diethylether, sammenlignet med den stærke hydrogenbinding i ethanol, resulterer i en lavere fordampningsentalpi. Dette betyder, at der kræves mindre varme for at fordampe diethylether end ethanol.
 Varme artikler
Varme artikler
-
 4 gennemprøvede strategier til at fremskynde kemiske reaktionerAf Vaibhav Rakesh – Opdateret 30. august 2022 Totojang/iStock/GettyImages En kemisk reaktion er drevet af kollisioner mellem reaktantmolekyler. En reaktions hastighed kan øges ved at manipulere fle
4 gennemprøvede strategier til at fremskynde kemiske reaktionerAf Vaibhav Rakesh – Opdateret 30. august 2022 Totojang/iStock/GettyImages En kemisk reaktion er drevet af kollisioner mellem reaktantmolekyler. En reaktions hastighed kan øges ved at manipulere fle -
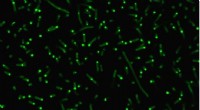 Forskere skaber kunstige organeller for at kontrollere cellulær adfærdIntrinsisk forstyrrede proteiner (fluorescerende grønt) klumper sig sammen i celler for at danne kunstige organeller. Kredit:Duke University Biomedicinske ingeniører ved Duke University har demons
Forskere skaber kunstige organeller for at kontrollere cellulær adfærdIntrinsisk forstyrrede proteiner (fluorescerende grønt) klumper sig sammen i celler for at danne kunstige organeller. Kredit:Duke University Biomedicinske ingeniører ved Duke University har demons -
 Integreret lab-on-a-chip bruger smartphone til hurtigt at opdage flere patogenerSystemet bruger en kommerciel smartphone til at erhverve og fortolke realtidsbilleder af en enzymatisk amplifikationsreaktion, der finder sted i en siliciummikrofluidisk chip, der genererer grøn fluor
Integreret lab-on-a-chip bruger smartphone til hurtigt at opdage flere patogenerSystemet bruger en kommerciel smartphone til at erhverve og fortolke realtidsbilleder af en enzymatisk amplifikationsreaktion, der finder sted i en siliciummikrofluidisk chip, der genererer grøn fluor -
 Forskere rapporterer om ny klasse af polyethylenkatalysatorerOlafs Daugulis, Robert A. Welch Chair of Chemistry ved University of Houston, ledet et team, der opdagede en ny klasse af katalysatorer til fremstilling af ultra-højvægts polyethylen. Kredit:Universit
Forskere rapporterer om ny klasse af polyethylenkatalysatorerOlafs Daugulis, Robert A. Welch Chair of Chemistry ved University of Houston, ledet et team, der opdagede en ny klasse af katalysatorer til fremstilling af ultra-højvægts polyethylen. Kredit:Universit
- En bjælke af sollys rammer Jorden på dette sted en næsten vinkelret vinkel?
- Sådan konverteres AMU til Mole
- Når selv at vinde er at tabe:De overraskende omkostninger ved at besejre Philip Morris over alminde…
- Hvordan kan tyngdekraften forårsage bevægelse af jordmaterialer?
- Sådan fungerer vinfremstilling
- At rense for længst glemte onlinekonti:Besværet værd?


