Forståelse af vand og iltattraktion:Van der Waals styrker
1. Van der Waals styrker:
* Disse er svage, kortrækkende attraktioner, der opstår på grund af midlertidige udsving i elektronfordelingen omkring molekyler.
* Selvom oxygen er et ikke-polært molekyle, oplever det stadig midlertidige, flygtige øjeblikke med ujævn elektronfordeling, hvilket skaber midlertidige dipoler.
* Disse midlertidige dipoler kan derefter inducere midlertidige dipoler i nabovandmolekyler, hvilket fører til en svag tiltrækning.
2. Dipol-inducerede dipol-interaktioner:
* Vandmolekyler er polære, hvilket betyder, at de har en permanent adskillelse af ladning med en positiv ende (brintatomer) og en negativ ende (iltatom).
* Denne permanente dipol i vand kan inducere en midlertidig dipol i iltmolekylet, selvom det er upolært.
* Den positive ende af vandmolekylet vil blive tiltrukket af den midlertidigt negative ende af iltmolekylet og omvendt.
Samlet set resulterer kombinationen af disse kræfter i en svag tiltrækning mellem vand- og iltmolekyler. Det er dog vigtigt at bemærke, at disse attraktioner er væsentligt svagere end de stærke brintbindinger, der eksisterer mellem vandmolekylerne selv.
Her er en forenklet analogi:
Forestil dig vandmolekyler som små magneter med en positiv og negativ ende. Iltmolekyler er som umagnetiserede metalgenstande. Selvom metalgenstandene ikke klæber stærkt til hinanden, kan de blive svagt tiltrukket af magneterne på grund af det inducerede magnetfelt.
 Varme artikler
Varme artikler
-
 Nye molekyler til OLED'er og lægemidlerFotografi af opløsninger af syntetiserede thiophenderivater i dioxan i dagslys og bestråling med en UV -lampe med en excitationsbølgelængde på 380 nm. Kredit:Nataliya Belskaya, Professor, UrFU Institu
Nye molekyler til OLED'er og lægemidlerFotografi af opløsninger af syntetiserede thiophenderivater i dioxan i dagslys og bestråling med en UV -lampe med en excitationsbølgelængde på 380 nm. Kredit:Nataliya Belskaya, Professor, UrFU Institu -
 Forskere opdager en unik strækbar lederAir Force Research Laboratory udviklede Polymerized Liquid Metal Network rupturing for at forvandle sig til et meget strækbart design, der autonomt øger ledningsevnen med belastning. Kredit:Second Bay
Forskere opdager en unik strækbar lederAir Force Research Laboratory udviklede Polymerized Liquid Metal Network rupturing for at forvandle sig til et meget strækbart design, der autonomt øger ledningsevnen med belastning. Kredit:Second Bay -
 Lille pumpe bygger polyrotaxaner med præcisionNorthwestern University forskere har udviklet den mest præcise måde at bygge polyrotaxaner på, en mekanisk låst polymer til glidering geler, batterielektrodematerialer og platforme til levering af læg
Lille pumpe bygger polyrotaxaner med præcisionNorthwestern University forskere har udviklet den mest præcise måde at bygge polyrotaxaner på, en mekanisk låst polymer til glidering geler, batterielektrodematerialer og platforme til levering af læg -
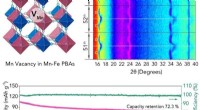 Forskning driver genopladelige batterier, der holder længereForskere udviklede et meget stabilt katodemateriale til natriumlagring. Kredit:SUTD Med den løbende forbedring af elektronik, udviklingen af højenergi-strømforsyninger er blevet et nøgleled i de
Forskning driver genopladelige batterier, der holder længereForskere udviklede et meget stabilt katodemateriale til natriumlagring. Kredit:SUTD Med den løbende forbedring af elektronik, udviklingen af højenergi-strømforsyninger er blevet et nøgleled i de
- Hvad er strukturen af vand og dets egenskaber betydning i menneskets krop?
- Hvorfor accelererer faldende genstande, da de kom tættere på jorden?
- Hvordan beregner jeg mængden af syre for at reducere vand pH?
- Hvilket læseniveau er nymåne?
- Hvordan understøttes Big Bang -teorien af observeret Doppler -skift af galakser?
- Undersøgelse har til formål at forbedre indfangning af vindkraft til energiproduktion


