Valenselektroner:Alkali- og jordalkalimetaller forklaret
Her er hvorfor:
* Alkalimetaller (gruppe 1): Disse grundstoffer har en elektron i deres yderste (valens) skal. De er meget reaktive og har en tendens til at miste denne elektron for at danne positivt ladede ioner med en ladning på +1. Eksempler omfatter lithium (Li), natrium (Na) og kalium (K).
* Alkaliske jordmetaller (gruppe 2): Disse grundstoffer har to elektroner i deres valensskal. De er også reaktive, men mindre end alkalimetaller. De har en tendens til at miste disse to elektroner for at danne positivt ladede ioner med en ladning på +2. Eksempler omfatter beryllium (Be), magnesium (Mg) og calcium (Ca).
Vigtig bemærkning: Mens antallet af valenselektroner definerer disse grupper, er der andre faktorer, der påvirker deres kemiske adfærd.
Sidste artikelBlandinger vs. løsninger:Forstå forskellene
Næste artikelGrapefruit Bloom:Hvad er det og er det sikkert at spise?
 Varme artikler
Varme artikler
-
 Et klarere overblik over, hvad der gør glas stiftEt team af forskere under ledelse af University of Tokyo bruger computersimuleringer til at undersøge stivheden af amorfe faste stoffer som glas. Kredit:Institute of Industrial Science, universitete
Et klarere overblik over, hvad der gør glas stiftEt team af forskere under ledelse af University of Tokyo bruger computersimuleringer til at undersøge stivheden af amorfe faste stoffer som glas. Kredit:Institute of Industrial Science, universitete -
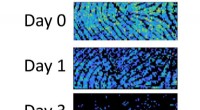 Rester i fingeraftryk indeholder spor af deres alderNiveauer af umættet triacylglycerol falder i fingeraftryk fra et individ fra dag 0 (øverst) til dag 1 (midten) og dag 3 (nederst). Kredit:Tilpasset fra Analytisk kemi 2020, DOI:10.1021/acs.analchem.
Rester i fingeraftryk indeholder spor af deres alderNiveauer af umættet triacylglycerol falder i fingeraftryk fra et individ fra dag 0 (øverst) til dag 1 (midten) og dag 3 (nederst). Kredit:Tilpasset fra Analytisk kemi 2020, DOI:10.1021/acs.analchem. -
 Ny software bringer cryo-EM-kort i lavere opløsning i fokusEt eksempel på den sekundære strukturdetektering i cryo-EM-densitetskort ved hjælp af Emap2Sec. Til venstre er et EM-kort over archaeal 20S proteasom (EMDB ID:EMD-1733). Til højre er detekteret sekund
Ny software bringer cryo-EM-kort i lavere opløsning i fokusEt eksempel på den sekundære strukturdetektering i cryo-EM-densitetskort ved hjælp af Emap2Sec. Til venstre er et EM-kort over archaeal 20S proteasom (EMDB ID:EMD-1733). Til højre er detekteret sekund -
 Undgå bobleproblemer:Undersøgelse af forholdet mellem bobler og elektrokemiFigur 1. Dannelse af bobler på overfladen af en elektrode. Kredit:University of Twente Bobler er kendt for at påvirke energi og masseoverførsel i gasudviklende elektroder. Mange elektrokemiske r
Undgå bobleproblemer:Undersøgelse af forholdet mellem bobler og elektrokemiFigur 1. Dannelse af bobler på overfladen af en elektrode. Kredit:University of Twente Bobler er kendt for at påvirke energi og masseoverførsel i gasudviklende elektroder. Mange elektrokemiske r
- Hvilket trofisk niveau er lav?
- Forureningsligatabeller for britiske byområder afslører det forventede og uventede
- Sådan gør du Multiplying & Factoring Polynomials
- Hvorfor opløses klorstabalisatoren ikke?
- Hvordan ville du beregne gravitationspotentialet energi fra en 2 kg flaske soda, der falder af køkk…
- Hvilket enzym slapper af eller fjerner forældrestrengen?


