Ethen vs. Ethan Opløselighed i svovlsyre:Forstå forskellen
1. Dobbeltbindingens rolle i Ethene
* Ethens dobbeltbinding: Ethen indeholder en carbon-carbon dobbeltbinding. Denne dobbeltbinding er elektronrig, hvilket betyder, at den har en høj koncentration af elektroner.
* Elektrofilt angreb: Koncentreret svovlsyre er en stærk elektrofil, hvilket betyder, at den tiltrækkes af elektronrige områder. Dobbeltbindingen i ethen fungerer som et sted for elektrofilt angreb af svovlsyren.
2. Reaktionen med svovlsyre
* Danning af et mellemprodukt: Den elektrofile svovlsyre angriber dobbeltbindingen i ethen, bryder dobbeltbindingen og danner en carbocation (et positivt ladet kulstofatom). Denne carbocation angribes derefter af sulfationen (SO4 2- ) til dannelse af en alkylhydrogensulfatester.
* Opløselighed: Denne alkylhydrogensulfatester er opløselig i koncentreret svovlsyre på grund af dens polære natur og dannelsen af hydrogenbindinger.
3. Hvorfor Ethane ikke opløses
* Ingen dobbeltbinding: Ethan har kun enkeltbindinger, hvilket betyder, at det mangler den elektronrige dobbeltbinding, der er afgørende for det elektrofile angreb af svovlsyre.
* Ikke-polær: Ethan er et ikke-polært molekyle. Koncentreret svovlsyre er et polært opløsningsmiddel, og "ligesom opløses ligesom." Manglen på polaritet i ethan forhindrer det i at opløses i den polære svovlsyre.
Opsummering:
Den vigtigste forskel ligger i reaktiviteten af de to molekyler. Ethens dobbeltbinding muliggør en reaktion med koncentreret svovlsyre, hvilket danner et opløseligt produkt. Ethan, der mangler en dobbeltbinding, reagerer ikke og forbliver derfor uopløseligt.
 Varme artikler
Varme artikler
-
 Biologer opdager carotenoidoverførsel mellem to proteinerCover art til denne artikel minder om coveret til albummet The Dark Side of the Moon af Pink Floyd. Det viser, hvor rødt, lilla, orange og violette proteiner kan fås fra et farveløst protein og en typ
Biologer opdager carotenoidoverførsel mellem to proteinerCover art til denne artikel minder om coveret til albummet The Dark Side of the Moon af Pink Floyd. Det viser, hvor rødt, lilla, orange og violette proteiner kan fås fra et farveløst protein og en typ -
 Hvordan forlænger man smøremidlernes brugstid?Uanset om det er i din bil eller en vindmølle, skum nedbryder det smøremiddel, der er nødvendigt for, at motorer kan arbejde effektivt. Kredit:Pixabay/phtorxp Vindmøller, der rager flere hundrede
Hvordan forlænger man smøremidlernes brugstid?Uanset om det er i din bil eller en vindmølle, skum nedbryder det smøremiddel, der er nødvendigt for, at motorer kan arbejde effektivt. Kredit:Pixabay/phtorxp Vindmøller, der rager flere hundrede -
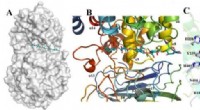 Strukturer i tang kaster lys over bæredygtighedOverfladerepræsentation og substratbindingsrille på Dp0100 Kredit:JI Shiqi Brunalger er ikke bare tang, der flyder i havet og floker svømmernes fødder - de indeholder også en hemmelighed. I sin ce
Strukturer i tang kaster lys over bæredygtighedOverfladerepræsentation og substratbindingsrille på Dp0100 Kredit:JI Shiqi Brunalger er ikke bare tang, der flyder i havet og floker svømmernes fødder - de indeholder også en hemmelighed. I sin ce -
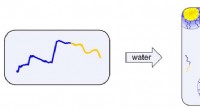 En ny, hurtigere måde at behandle diblok-polymermaterialer påDen blå ende af hver kæde er opløselig i vand, mens den gule ende ikke er det. De gule ender samler sig i et forsøg på at adskille fra vandet. Disse kugleformede klynger kaldes miceller. Kredit:Connor
En ny, hurtigere måde at behandle diblok-polymermaterialer påDen blå ende af hver kæde er opløselig i vand, mens den gule ende ikke er det. De gule ender samler sig i et forsøg på at adskille fra vandet. Disse kugleformede klynger kaldes miceller. Kredit:Connor
- Inkblot test med AI:OMG, gadestikkeri? Ingen, blomst og fløjte
- 90% af Floridianerne tror, at klimaændringer sker:Undersøgelse
- Hvordan er inertien af et objekt relateret til dets masse?
- Smart magnetisk materiale i flere lag fungerer som en elektrisk kontakt
- Resumér hierarkiet af organisation, der findes i komplekse multicellulære organismer?
- Hvorfor er brom en bedre afgangsgruppe end klor?


