Ionisk binding:Forståelse af valenselektronoverførsel
* Metaller har tendens til at miste deres valenselektroner for at opnå en stabil elektronkonfiguration, normalt en oktet (8 elektroner i den yderste skal).
* Ikke-metaller tendens til at få valenselektroner for også at opnå en stabil oktet.
Sådan fungerer det:
1. Elektronoverførsel: Når et metalatom interagerer med et ikke-metalatom, *donerer* metalatomet sine valenselektroner til ikke-metalatomet.
2. Danning af ioner: Denne overførsel skaber to modsat ladede ioner:
* Metalatomet bliver en kation (positivt ladet ion), fordi den har mistet elektroner.
* Ikke-metalatomet bliver en anion (negativt ladet ion), fordi den har fået elektroner.
3. Elektrostatisk tiltrækning: Den stærke elektrostatiske tiltrækning mellem de modsat ladede ioner holder dem sammen og danner ionbindingen.
Eksempel:Natriumchlorid (NaCl)
* Natrium (Na) har 1 valenselektron. Den mister denne elektron og bliver til en natriumkation (Na+).
* Klor (Cl) har 7 valenselektroner. Den får en elektron til at blive en chloridanion (Cl-).
* De modsat ladede ioner (Na+ og Cl-) holdes sammen af den elektrostatiske tiltrækning og danner den ioniske forbindelse natriumchlorid.
Nøglepunkter:
* Ionbindinger involverer fuldstændig overførsel af valenselektroner, ikke deling.
* De resulterende ioner har en stabil elektronkonfiguration, normalt en oktet.
* Den stærke elektrostatiske tiltrækning mellem ionerne er drivkraften bag bindingen.
 Varme artikler
Varme artikler
-
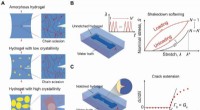 Anti-træthedsbrud hydrogelerDesignprincip for anti-træthedsbrud-hydrogeler. (A) Illustration af udmattelsesrevneudbredelse i en amorf hydrogel og i hydrogeler med lave og høje krystalliniteter under cykliske belastninger. De gul
Anti-træthedsbrud hydrogelerDesignprincip for anti-træthedsbrud-hydrogeler. (A) Illustration af udmattelsesrevneudbredelse i en amorf hydrogel og i hydrogeler med lave og høje krystalliniteter under cykliske belastninger. De gul -
 Model forudsiger polymer mademballager tilbøjelighed til at absorbere aromamolekyler fra deres indh…Kredit:CC0 Public Domain Dine yndlingsfødevarer og drikkevarer vil snart kunne smage endnu bedre, takket være nye beregninger udviklet på A*STAR. En væsentlig kilde til tab af smag til mad og drik
Model forudsiger polymer mademballager tilbøjelighed til at absorbere aromamolekyler fra deres indh…Kredit:CC0 Public Domain Dine yndlingsfødevarer og drikkevarer vil snart kunne smage endnu bedre, takket være nye beregninger udviklet på A*STAR. En væsentlig kilde til tab af smag til mad og drik -
 Ekstreme forhold i halvledereNærbillede af det eksperimentelle setup i University of Konstanz højfelts Terahertz-laboratorium. Under eksperimentets ekstreme forhold, et klart rødt skær kan ses at udgå fra galliumarsenidkrystal, d
Ekstreme forhold i halvledereNærbillede af det eksperimentelle setup i University of Konstanz højfelts Terahertz-laboratorium. Under eksperimentets ekstreme forhold, et klart rødt skær kan ses at udgå fra galliumarsenidkrystal, d -
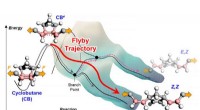 Kemiske reaktioner bryder fri fra energibarrierer ved at bruge flyby-banerEn illustration, der viser et molekyles bevægelse hen over en potentiel energioverflade på den måde, vandrere følger konturkortet over bjerge og dale langs en sti. Når der påføres en mekanisk kraft, e
Kemiske reaktioner bryder fri fra energibarrierer ved at bruge flyby-banerEn illustration, der viser et molekyles bevægelse hen over en potentiel energioverflade på den måde, vandrere følger konturkortet over bjerge og dale langs en sti. Når der påføres en mekanisk kraft, e
- Hvordan påvirker ændringer i temperaturen volumen af en gas?
- Sådan beregnes et flytende område
- Hvad er reaktionen af B-naphthol med natriumhydroxid?
- Tyndtarmspermeable peptider letter optagelsen af fordøjelseskanalen
- Hvad dannes ved erosion af bløde stenformationer, der flyder grundvand?
- Hvorfor er lys ikke synlig gennem et bøjet rør?


