Valens og reaktivitet:Sammenligning af elementer med 7 og 8 valenselektroner
* Oktetregel: Atomer stræber efter at opnå en stabil elektronkonfiguration ligesom ædelgasserne, der har en fuld ydre skal (8 valenselektroner).
* Reaktivitet: Grundstoffer med 7 valenselektroner er kun én elektron væk fra at opnå en hel oktet. Dette gør dem meget reaktive, da de let får en elektron til at færdiggøre deres ydre skal.
* Eksempel: Halogener (som klor, fluor, brom) er i gruppe 17 i det periodiske system og har 7 valenselektroner. De er meget reaktive ikke-metaller.
* Stabilitet: Grundstoffer med 8 valenselektroner har en fuld ydre skal og er meget stabile, hvilket betyder, at de ikke er reaktive. Det er derfor ædelgasser er inerte.
Sammenfattende er grundstoffer med 7 valenselektroner meget reaktive, fordi de er én elektron væk fra at opnå en stabil oktet, mens grundstoffer med 8 valenselektroner allerede er stabile og ikke-reaktive.
 Varme artikler
Varme artikler
-
 Førsteklasses YEATS-hæmmere, der viser løfte om leukæmibehandlingDr. Xiang David Li og hans forskningsgruppe ved HKU Institut for Kemi. Kredit:@The University of Hong Kong Et forskerhold ledet af Dr. Xiang David Li fra Institut for Kemi ved University of Hong K
Førsteklasses YEATS-hæmmere, der viser løfte om leukæmibehandlingDr. Xiang David Li og hans forskningsgruppe ved HKU Institut for Kemi. Kredit:@The University of Hong Kong Et forskerhold ledet af Dr. Xiang David Li fra Institut for Kemi ved University of Hong K -
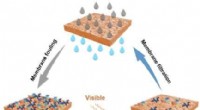 Forskere udvikler N-dopede selvrensende membraner, der bruger bestråling af synligt lysSkematisk diagram af N-TiO 2 og TiO 2 overtrukket membranforberedelse og mekanisme for synligt lysaktiveret fotokatalyse til begroningsbegrænsning. Kredit:ZHANG Huiru Forskere fra Institute of
Forskere udvikler N-dopede selvrensende membraner, der bruger bestråling af synligt lysSkematisk diagram af N-TiO 2 og TiO 2 overtrukket membranforberedelse og mekanisme for synligt lysaktiveret fotokatalyse til begroningsbegrænsning. Kredit:ZHANG Huiru Forskere fra Institute of -
 Ny teori for, hvordan snefnug vokserKredit:Pixabay/CC0 Public Domain Forskere har opdaget, hvad der driver det sarte og komplekse mikrokosmos af små terrasser, pyramider og kratere fundet på overfladen af is. Disse miniature struk
Ny teori for, hvordan snefnug vokserKredit:Pixabay/CC0 Public Domain Forskere har opdaget, hvad der driver det sarte og komplekse mikrokosmos af små terrasser, pyramider og kratere fundet på overfladen af is. Disse miniature struk -
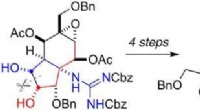 Fremstilling af pufferfisktoksin i en kolbeKredit:Angewandte Chemie I Japan, puffer fisk betragtes som en delikatesse, men kildren til smagsløgene kommer med en kildren til nerverne:fugu indeholder tetrodotoxin, et stærkt nervegift. I lave
Fremstilling af pufferfisktoksin i en kolbeKredit:Angewandte Chemie I Japan, puffer fisk betragtes som en delikatesse, men kildren til smagsløgene kommer med en kildren til nerverne:fugu indeholder tetrodotoxin, et stærkt nervegift. I lave
- Eksperter advarer Australien mod fare for tørke, stigende vandstand
- Hvordan produceres og tranmitteres lydenergi?
- Hvad Canada ved om fødevarekriser kan hjælpe med at forhindre mangel og beskytte arbejdere under c…
- En pære omdanner elektrisk energi til både varme og energi-?
- Ændringer i NFL afspejler ændringer på moderne arbejdspladser, siger papiret
- Hvilket domæne er bakterier?


