Arsen Pentachlorid (AsCl₅) Hybridisering:Forstå sp³d²
* Elektronkonfiguration: Arsen har 5 valenselektroner (4s² 4p³).
* Binding: I AsCl₅ danner arsen fem enkeltbindinger med fem chloratomer.
* Hybridisering: For at rumme de fem bindinger har arsen brug for fem orbitaler. Dette opnås ved hybridisering, hvor en s orbitaler, tre p orbitaler og to d orbitaler kombineres for at danne fem sp³d² hybrid orbitaler.
* Geometri: Sp³d²-hybridiseringen resulterer i en trigonal bipyramidal molekylær geometri.
Opsummering: Det centrale arsenatom i AsCl₅ bruger sine fem valenselektroner og fem hybridorbitaler (sp³d²) til at danne fem enkelt kovalente bindinger med fem chloratomer, hvilket resulterer i en trigonal bipyramidal struktur.
 Varme artikler
Varme artikler
-
 Hvordan kemiske bindinger brydes og reformeres:Videnskaben om endoterme og eksoterme reaktionerblanscape/iStock/GettyImages I hver kemisk reaktion spaltes etablerede molekylære bindinger, mens nye bindinger dannes. Almindelige eksempler omfatter forbrænding, reduktion og nedbør. Omlejringen af
Hvordan kemiske bindinger brydes og reformeres:Videnskaben om endoterme og eksoterme reaktionerblanscape/iStock/GettyImages I hver kemisk reaktion spaltes etablerede molekylære bindinger, mens nye bindinger dannes. Almindelige eksempler omfatter forbrænding, reduktion og nedbør. Omlejringen af -
 En venligere måde at håndtere nitratforurening påKredit:CC0 Public Domain At lære af naturen, forskere fra Center for Sustainable Resource Science i Japan og Korean Basic Science Institute (KBSI) har fundet en katalysator, der effektivt omdanner
En venligere måde at håndtere nitratforurening påKredit:CC0 Public Domain At lære af naturen, forskere fra Center for Sustainable Resource Science i Japan og Korean Basic Science Institute (KBSI) har fundet en katalysator, der effektivt omdanner -
 Bakterieovertrukne nanofiberelektroder fordøjer forurenende stofferCarbon nanofibre belagt med PEDOT i et scanning elektronmikroskop billede. Kredit:Juan Guzman og Meryem Pehlivaner/Provided Cornell-materialeforskere og bioelektrokemiske ingeniører kan have skabt
Bakterieovertrukne nanofiberelektroder fordøjer forurenende stofferCarbon nanofibre belagt med PEDOT i et scanning elektronmikroskop billede. Kredit:Juan Guzman og Meryem Pehlivaner/Provided Cornell-materialeforskere og bioelektrokemiske ingeniører kan have skabt -
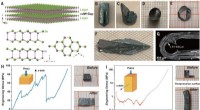 Forskere finder, at krystaller af indiumselenid har enestående fleksibilitetDeformerbarhed af InSe enkeltkrystaller. (A) Krystalstruktur af β-InSe og projektionen på (110) og (001) planerne. (B) Som-vokset krystal og (C) spaltningsoverflade. (D til F) InSe enkeltkrystal omdan
Forskere finder, at krystaller af indiumselenid har enestående fleksibilitetDeformerbarhed af InSe enkeltkrystaller. (A) Krystalstruktur af β-InSe og projektionen på (110) og (001) planerne. (B) Som-vokset krystal og (C) spaltningsoverflade. (D til F) InSe enkeltkrystal omdan


